專注於開發和商業化中樞神經系統(CNS)疾病新型療法的生物製藥公司 Axsome Therapeutics, Inc. 周三宣佈,美國食品藥品監督管理局(FDA)已對其提交的、旨在擴大其抑鬱症療法AXS-05(商品名:Auvelity)適應症至阿爾茨海默病激越症狀的上市申請授予優先審評資格。該公司在一份聲明中表示,針對AXS-05的補充新藥申請,FDA已將2026年4月30日設定為目標審評完成日期。
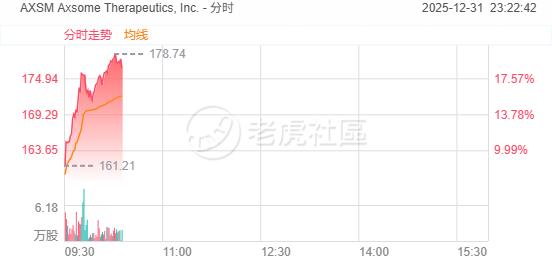
Axsome Therapeutics盤初拉升大升逾19%。
2022年,FDA批准AXS-05用於治療成人重度抑鬱症。2020年,FDA授予該藥物治療阿爾茨海默病激越症狀的突破性療法資格。資料顯示,阿爾茨海默病(AD),又稱老年性癡呆,是一種常見的神經系統退行性疾病。其發病機制複雜,主要表現為記憶力下降、認知功能減退、行為異常等。據報道,超過一半以上的AD患者存在激越症狀,其特徵是情緒困擾、言語和身體攻擊性、破壞性易怒和脫抑制。激越是阿爾茨海默病(AD)患者的一種神經精神症狀,這種情況通常在AD病程早期就開始出現並持續存在,這會增加醫療保健的費用,並顯著增加護理人員的負擔和患者的痛苦。
AXS-05(右美沙芬-安非他酮)是一種口服N-甲基-D-天冬氨酸受體拮抗劑、sigma-1激動劑和氨基酮CYP2D6抑制劑。AXS-05利用右美沙芬和安非他酮的專利配方和劑量,以及Axsome的代謝抑制技術,來調節成分的輸送。AXS-05的右美沙芬成分是非競爭性NMDA受體拮抗劑,也稱為穀氨酸受體調節劑和σ-1受體激動劑。AXS-05的安非他酮成分用於增加右美沙芬的生物利用度,並且是去甲腎上腺素和多巴胺再攝取抑制劑。這種新型療法有望改善以情緒困擾、言語和身體攻擊、破壞性易怒和脫抑制為特徵的AD激越。
Axsome首席執行官Herriot Tabuteau表示:「我們非常高興FDA受理並授予了我們的補充新藥申請優先審評資格,該申請旨在將AXS-05用於治療阿爾茨海默病激越症狀。我們期待在接下來的審評階段繼續與FDA保持合作。」