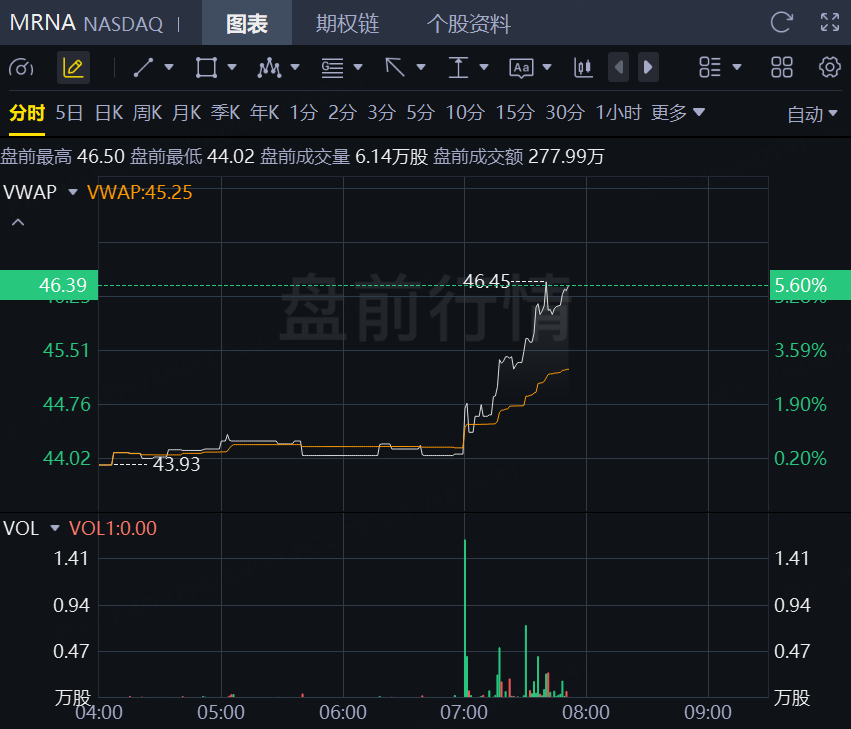
2月18日,Moderna盤前升逾5%!此前該公司宣佈美國食品藥品監督管理局(FDA)已同意審查其在研季節性流感疫苗mRNA-1010的生物製品許可申請。
FDA的這一決定是在A類會議後做出的,Moderna在會上提出了該候選疫苗的修訂監管方案。該公司根據《處方藥用戶費用法案》(PDUFA)獲得的目標日期為2026年8月5日,這為FDA的審查流程設定了時間表。
Moderna的修訂方案尋求對50至64歲成年人的完全批准,以及對65歲及以上人群的加速批准,並承諾在上市後要求中對老年人進行額外研究。如果獲得批准,該疫苗將在2026/2027年流感季節向50歲及以上的美國成年人提供。
"我們感謝FDA在富有建設性的A類會議中的參與,以及其同意推進我們的申請審查,"Moderna首席執行官Stéphane Bancel表示。"在FDA批准的前提下,我們期待在今年晚些時候提供我們的流感疫苗,讓美國老年人能夠獲得保護自己免受流感侵害的新選擇。"
FDA決定審查該申請是在此前發出拒絕受理函之後做出的,這促使Moderna與監管機構進行溝通並提出修訂方案。mRNA-1010疫苗也已被歐洲、加拿大和澳大利亞接受審查,並計劃在2026年全年提交更多申請。
Moderna預計mRNA-1010將在2026年獲得首批潛在批准,具體取決於各個市場正在進行的監管審查。