據IPO早知道消息,維立志博於2025年6月4日更新招股書,繼續推進港交所主板上市進程,摩根士丹利和中信證券擔任聯席保薦人。
這意味着,維立志博或將成為「國內TCE領域第一股」。
維立志博成立於2012年,是一家臨牀階段生物科技公司,專注於發現、開發及商業化用於治療中國及全球腫瘤、自身免疫性疾病及其他重大疾病的創新療法。
截至2025年5月28日,維立志博管線涵蓋14款候選藥物,包括針對腫瘤的3款單克隆抗體、4款雙特異性抗體、2款抗體偶聯藥物(ADC)及1款雙特異性融合蛋白,以及針對自免疾病的1款雙特異性融合蛋白及1款三特異性抗體。
值得一提的是,維立志博基於LeadsBody™專有技術平台,已構建覆蓋血液瘤、實體瘤及自免三大疾病領域的TCE產品矩陣。
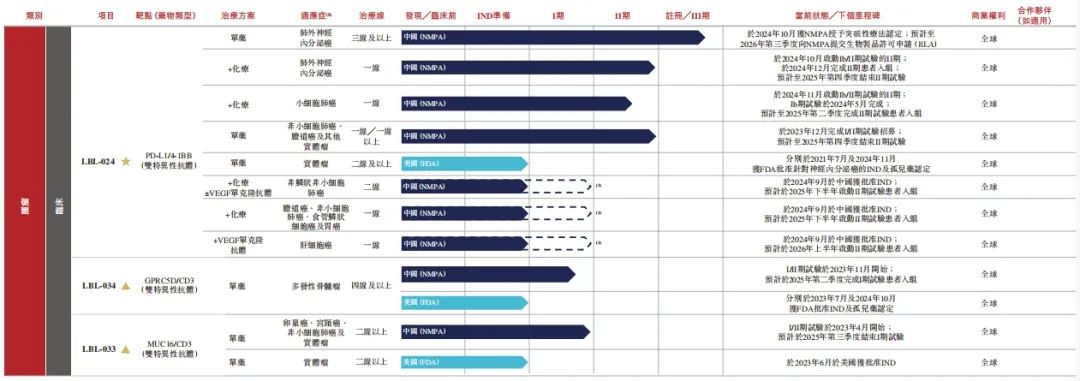
其中,維立志博有6款產品已進入臨牀階段,包括1款核心產品及3款主要產品。
核心產品LBL-024為一款處於註冊臨牀階段的PD-L1與4-1BB雙特異性抗體,是全球首個進入註冊臨牀試驗階段的4-1BB靶向候選藥物,旨在填補晚期肺外神經內分泌癌(EP-NEC)治療的重大缺口。
該藥物還獲得了中國國家藥監局和FDA的突破性療法認定及孤兒藥認定,目前正在進行多項針對晚期肺外神經內分泌癌、小細胞肺癌、膽道癌、非小細胞肺癌及其他實體瘤的臨牀試驗,預計2029年提交肺外神經內分泌癌及小細胞肺癌一線治療的生物製品許可申請(BLA)。
同時,維立志博主要產品LBL-034,是全球臨牀進度第二領先的靶向GPRC5D的CD3 TCE,在臨牀前研究中展現出良好療效信號和較高的GPRC5D結合親和力及效力,同時也降低了T細胞免疫疲勞風險及對健康細胞的損害。
在複發性/難治性多發性骨髓瘤單藥療法的I/II期試驗中表現出了優異的客觀緩解率等數據,有望為多發性骨髓瘤的治療提供更優越的療效及更長的治療窗口期。
主要產品LBL-033,是全球僅有的兩款已進入臨牀階段的MUC16/CD3雙特異性TCE抗體之一,用於治療MUC16高表達的實體瘤,特別是卵巢癌、宮頸癌及子宮內膜癌等婦科癌症。
其獨特的分子設計可提高靶向特異性,減少靶向非腫瘤毒性,降低有害免疫應答的風險,在單藥療法的I/II期試驗中初步顯示出良好的療效和安全性。
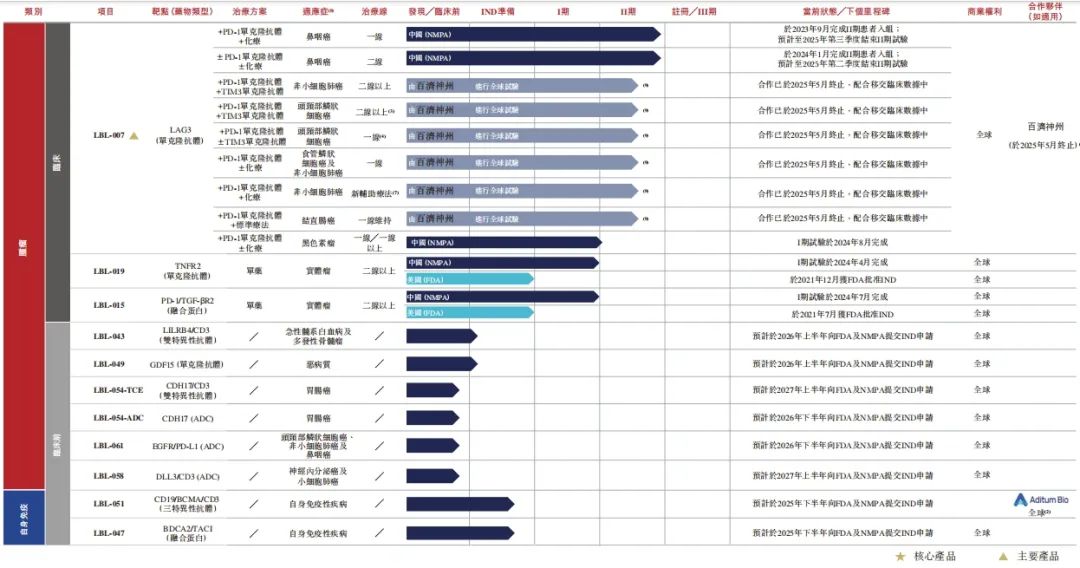
另一款主要產品LBL-007,在全球處於臨牀階段的LAG3靶向單克隆抗體中臨牀進度位居前三,是首款被證實對鼻咽癌有效的同類抗體。
在聯合替雷利珠單抗治療一線鼻咽癌患者的II期試驗中,展現出較高的客觀緩解率、疾病控制率等積極數據,有望為鼻咽癌患者提供更有效的治療選擇。
在出海合作方面,2024年11月,維立志博與Aditum Bio就LBL-051(CD19xBCMAxCD3三特異性TCE抗體)達成NewCo合作,總價值高達6.14億美元。
成立至今,維立志博獲得了恩然創投、正心谷、漢康資本、懷格資本、新希望醫療、龍磐投資、華方資本、新絲路資本、國泓、深創投等機構的投資,於2024年完成的C+輪投後估值為31.3億元。