1月5日據國家藥監局官網消息,我國國產體外膜肺氧合治療(ECMO)產品獲批上市。
國家藥監局表示,根據疫情防控工作需要,為確保新型冠狀病毒肺炎重症患者治療需要,2023年1月4日,國家藥監局經審查,應急批准深圳漢諾醫療科技有限公司體外心肺支持輔助設備、一次性使用膜式氧合器套包註冊申請,二者配合使用,用於急性呼吸衰竭或急性心肺功能衰竭、其他治療方法難以控制並有可預見的病情持續惡化或死亡風險的成人患者。作為國產首個ECMO設備和耗材套包,上述產品具有自主知識產權,性能指標基本達到國際同類產品水平。
其中,體外心肺支持輔助設備由主機、泵驅動裝置、緊急泵驅動裝置、備用電池、流量氣泡傳感器等組成。一次性使用膜式氧合器套包由膜式氧合器及動靜脈管路組件(含離心泵泵頭),預充管路組件,配件包組件和氧氣管路組成。
公告稱,ECMO產品作為常規治療無效的危重型新型冠狀病毒肺炎患者的挽救性治療設備,是《新型冠狀病毒肺炎診療方案》中明確的治療措施,國產產品的上市對於滿足臨牀急需,保障新冠疫情重症患者治療,確保疫情防控「保健康、防重症」目標落實,將發揮重要作用。
在該產品的註冊申報過程中,國家藥監局按照「統一指揮、早期介入、快速高效、科學審批」的原則,成立應急審評工作組,專人負責、全程指導、發布技術審查指導原則,加大產品註冊申報指導,加快審評審批進程,在保證安全、有效的基礎上推動產品儘快上市,滿足疫情防控工作急需。
藥品監督管理部門將加強該產品上市後監管,保護患者用械安全。
ECMO能做什麼呢?
據悉,ECMO 就是應用血泵產生動力,經過靜脈插管建立血管通路,把血引出,然後經過膜肺(也就是常說的「人工肺」)。膜肺在連接氧氣後,氧就能彌散到血,二氧化碳也能通過膜肺排出,膜肺把靜脈血變成動脈血。這動脈血再通過血管插管的建立的灌注通路,回到人體。ECMO只是代替了呼吸功能(VV)和或心肺功能(VA),而且只能是短時間的,並不能完全取代我們的肺或心臟。
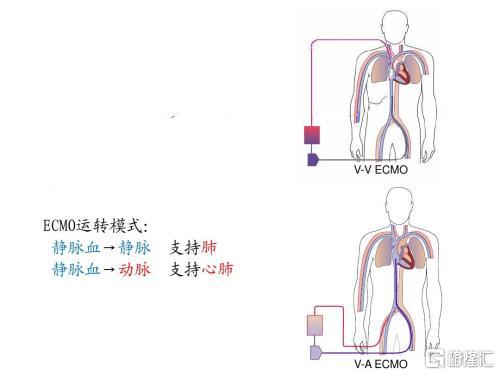
對於受新冠病毒感染的重症患者,利用ECMO設備可以暫時代替人的心和肺起作用,等待心肺功能恢復。
2020年初新冠疫情暴發後,多家醫院使用ECMO救治新冠重症患者,但因設備短缺引起廣泛關注。
據了解,一般只有三級醫院纔會配備ECMO,且一家醫院通常只會配備1~2台。
中國生物醫學工程會體外循環分會2018年的統計數據顯示,我國僅有260家醫院有ECMO設備,全國僅有約400台ECMO。就算是在美國,當時也僅有264家ECMO中心,全球的ECMO設備存量僅有1200台。
國產ECMO產品獲批上市,或打破進口壟斷
此次國產ECMO獲批上市之前,國內醫療機構使用的ECMO,主要依靠進口。縱觀全球範圍內,可以生產ECMO的廠家寥寥無幾,目前主要是邁柯唯、美敦力和理諾琺這些跨國企業包攬了大部分的市場份額,佔據全球ECMO設備市場的前三名。
ECMO材料生產壁壘高,臨牀使用制約、市場需求等多重因素,嚴重依賴進口,是價格始終高居不下的原因之一。
高昂的價格也是ECMO設備短缺的原因之一。華西證券研報顯示,國內ECMO設備價格區間為100萬元~300萬元,均價為165萬元,移動ECMO價格約300萬元/台。中國政府採購網在2022年6月23日發布的採購公告顯示,復旦大學附屬華山醫院ECMO採購的中標金額為250萬元/台。同時,實際治療過程中治療費用昂貴,國內治療費用開機5萬元起,國外需10萬美元。
天眼查App顯示,深圳漢諾醫療科技有限公司成立於2018年5月,法定代表人為李鳴濤,註冊資本約1338.4萬人民幣,由LI YIJIANG、深圳邁瑞股權投資基金股份有限公司等共同持股。資料顯示,公司專注於體外循環、體外生命支持類醫療設備和耗材,全鏈條產品的研發、製造、臨牀驗證和全球銷售,自主研製的體外膜肺氧合ECMO產品擁有完全自主知識產權與核心創新技術,該產品系列有望在短期內打破國外目前100%的市場壟斷,實現中國在體外生命支持技術領域從零到一的國產化突破。