今日,中國國家藥監局藥品審評中心(CDE)官網最新公示,禮來公司(LLY.US)(Eli Lilly and Company)申報的米吉珠單抗注射液(mirikizumab)以及其皮下注射劑型的新適應症上市申請獲得受理。公開資料顯示,這是禮來研發的IL-23抑制劑,該療法曾被Evalulate列為10大潛在重磅療法之一。該藥在中國的首個上市申請於去年10月獲得CDE受理,針對適應症為克羅恩病。根據公開資料推測,本次該藥申報上市的適應症為可能為治療中重度活動性潰瘍性結腸炎(UC)成人患者。
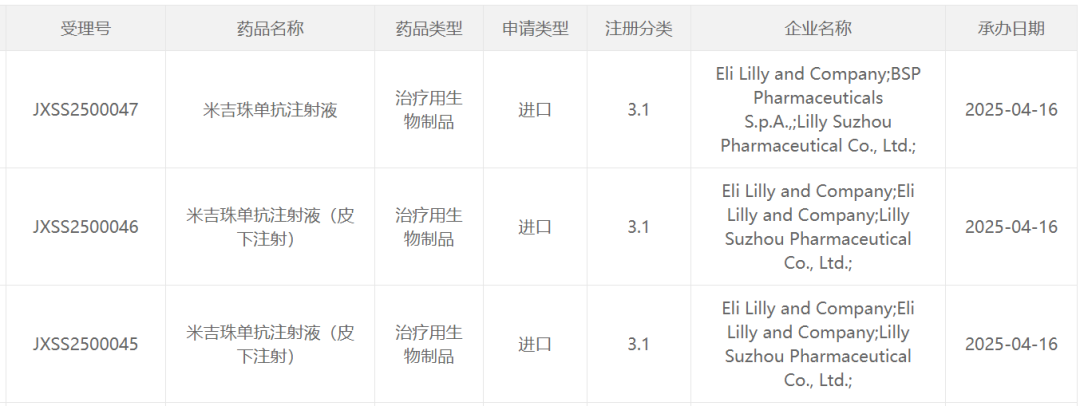 截圖來源:CDE官網
截圖來源:CDE官網米吉珠單抗是一款人源化IgG4單克隆抗體,可與IL-23的p19亞基結合,阻斷IL-23介導的炎症反應。作為一種炎性細胞因子,IL-23參與了多個炎症相關的生理過程,被認為與許多免疫介導的慢性疾病有關,也因此成為了許多自身免疫性疾病的治療靶點。
2023年10月,美國FDA批准米吉珠單抗用於治療中重度活動性潰瘍性結腸炎(UC)成人患者。根據禮來此前新聞稿,這是首個用於治療這一患者羣體的IL-23p19拮抗劑。該產品治療潰瘍性結腸炎開始時靜脈輸注300毫克,每4周輸注一次,共輸注3次,在維持治療期間,每4周進行兩次100毫克皮下注射。2025年1月,米吉珠單抗再次獲FDA批准,用於治療成人中度至重度活動性克羅恩病(CD)。
海量資訊、精準解讀,盡在新浪財經APP