在全球創新藥投資邏輯向「真創新、高壁壘」切換的背景下,中國創新藥企在雙抗等前沿領域持續突破,開始在國際頂級學術舞台展露鋒芒。
繼去年美國臨床腫瘤學會(ASCO)年會以單藥療法驚豔亮相後,維立志博研發的抗PD-L1/4-1BB雙抗LBL-024在2025年ASCO舞台再獲突破性驗證。
從二線單藥治療到一線聯合化療的臨床數據連番釋放,本質上亦映射出中國創新藥企在雙抗領域從「技術可行性驗證」到「臨床價值深挖」的進階能力。
那麼站在投資者的視角而言,應當如何來看待這一最新臨床數據的表現?該數據對於維立志博又有何意義?
潛在全球首創,真正源頭創新錨定臨床價值
不同於傳統單抗療法的線性突破邏輯,LBL-024通過PD-L1靶向鎖定腫瘤微環境、4-1BB共刺激激活T細胞的"雙引擎"設計,實現腫瘤微環境裏的條件激活T細胞,開創性地解決了4-1BB靶點系統性激活引發肝毒性的痛點。這種腫瘤微環境精準調控機制,使其成為全球首個有望實現4-1BB靶點商業化突破的免疫療法。
2024 ASCO大會,LBL-024單藥在針對二線治療、三線及以上治療肺外神經內分泌癌(EP-NEC)的患者中,展現出良好的安全性和強有力的有效信號。
數據顯示,6個月總生存期比率(OS)分別為61.7%、72.7%和52.0%。在22例PD-L1陰性(CPS<1)的患者中,總體客觀緩解率(ORR)為54.5%,且無論PD-L1在腫瘤組織中的表達如何,患者都可以從LBL-024治療中獲益。
2025 ASCO盛會,LBL-024聯合化療作為初治晚期EP-NEC患者的一線治療結果入選大會發言,再次印證了其協同作用機制為這類難治性腫瘤提供了突破性治療選擇。
在療效性上,EP-NEC患者的ORR達75.0%,疾病控制率(DCR)為92.3%,顯著優於歷史數據中單純化療的ORR。其中15mg/kg劑量優化組裏,EP-NEC可評估患者ORR為83.3%,DCR達100%。
在安全性上,LBL-024聯合化療耐受性良好,所有劑量組均未報告劑量限制性毒性(DLT),治療相關不良事件以1-2級為主(如中性粒細胞減少、貧血)。
這種增效不增毒的特性,使其在晚期EP-NEC治療領域形成「單藥破局生存困境、聯合重塑一線治療」的立體化競爭優勢,為後續全球多中心臨床推進奠定基礎。
目前,LBL-024已在中美兩大核心市場獲得監管突破。其中,中國藥監局授予其治療EP-NEC的突破性療法認定,FDA則批准針對神經內分泌癌的孤兒藥資格。
在筆者看來,LBL-024的連續學術驗證,既證明了中國創新藥企在複雜靶點組合與臨床開發策略上的體系化能力,也為破解實體瘤治療耐藥困境提供了可複製的技術模板,標誌着中國創新藥企在腫瘤免疫治療領域實現從0到1的源頭創新。
此前國內PD-1/PD-L1等熱門靶點的研發多集中於Fast-follow模式,雖在商業化上取得規模突破,但本質上仍是對海外技術路徑的迭代優化。而LBL-024通過自主設計的雙抗結構,在全球範圍內首次攻克4-1BB靶點系統性激活的肝毒性難題,有望成為繼CTLA-4、PD-1/L1和LAG-3後全球第四個免疫檢查點有效治療腫瘤的藥物。LBL-024的成功將重新定義中國創新藥在全球產業鏈中的角色,不再是跟隨者而是源頭創新的引領者。
單點突破到多點開花,多癌種延伸構建增長飛輪
在確立EP-NEC治療領域的優勢地位後,基於雙抗技術的廣譜癌症治療潛力和對PD-1/PD-L1無效患者羣體的覆蓋,LBL-024「一藥多癌」的獨特商業價值也正不斷釋放。
目前,維立志博正以LBL-024為核心,啓動小細胞肺癌、卵巢癌、膽道癌、非小細胞肺癌及其他實體瘤療效的臨床研究,並計劃將進一步挖掘食管鱗狀細胞癌、胃癌及肝細胞癌等更多高發癌症領域,持續拓寬適應症邊界。
以小細胞肺癌臨床為例,截至2025年2月14日,在LBL-024針對治療一線小細胞肺癌的臨床Ib/II期試驗裏,19名可評估患者中,總體ORR達84.2%,DCR達100%,展現出良好的安全性和初步療效。
這種戰略選擇的底層邏輯,與4-1BB靶點藥物的市場爆發形成共振,持續增長的市場需求為LBL-024提供了可觀的商業化空間。
從患者基數來看,據弗若斯特沙利文預測,這類藥物瞄準的不僅是全球年發病率超8萬例的肺外神經內分泌癌領域,更劍指小細胞肺癌(全球年發病人數43萬例)、非小細胞肺癌(230萬例)等仍有龐大尚未被滿足治療需求的市場。

市場規模也已顯現出清晰的增長曲線。
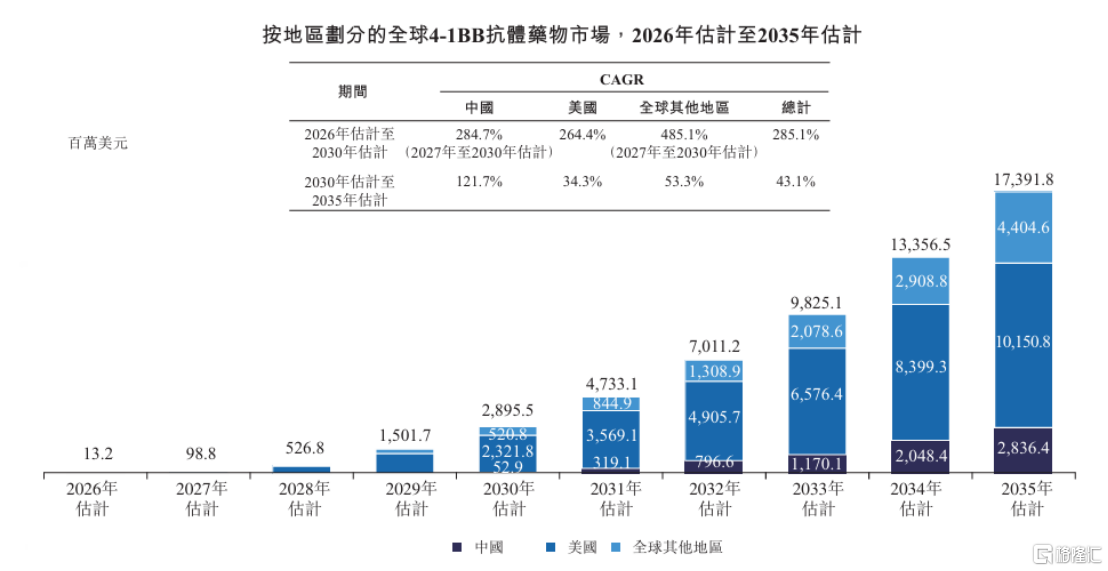
弗若斯特沙利文數據顯示,預計全球4-1BB抗體市場於2026年、2030年及2035年將分別達至13.2百萬美元、29億美元及174億美元,CAGR於2026年至2030年為285.1%及於2030年至2035年為43.1%。
若LBL-024作為全球首個靶向4-1BB的FIC藥物成功上市,其憑藉獨佔性和臨床優勢,將享有更高的定價權和市場滲透率,潛在市場規模亦有望高於傳統Me-too藥物。
隨着後續LBL-024在更多癌種上臨床價值的驗證,其商業生命周期的延展性亦有望在不同治療領域的數據共振中形成自我強化的增長飛輪。
結語
作為潛在全球首創的4-1BB腫瘤免疫治療藥物,LBL-024的突破性進展徹底打破了中國創新藥只能做Me-too/Me-better的固有印象。4-1BB靶點的成藥性驗證,不僅為維立志博帶來獨佔性商業紅利,更標誌着中國創新藥企在靶點選擇、分子設計、臨床開發等全鏈條上具備了與全球頂尖藥企同台競技的硬核實力。
而對於投資者而言,LBL-024展現的不僅是單一產品的臨床優勢,更折射出維立志博在靶點組合創新、臨床開發策略和全球化佈局上的體系化能力。
除LBL-024外,維立志博LBL-034等多款極具全球競爭力的差異化創新藥物品的協同推進,廣泛覆蓋腫瘤、自身免疫性疾病及其他重大疾病,更構建了風險分散、價值疊加的創新矩陣。
現如今,在資本市場更加關注企業底層創新能力的趨勢下,這種兼具廣度與深度的研發生態,已成為公司穿越行業周期、實現持續增長的核心競爭力。