近日,作為腫瘤領域規模盛大的年度學術盛會——2025年美國臨床腫瘤學會(ASCO)年會正如火如荼進行中,受到國際學界廣泛關注,而全球二級市場投資者也在積極挖掘其中的投資機會。
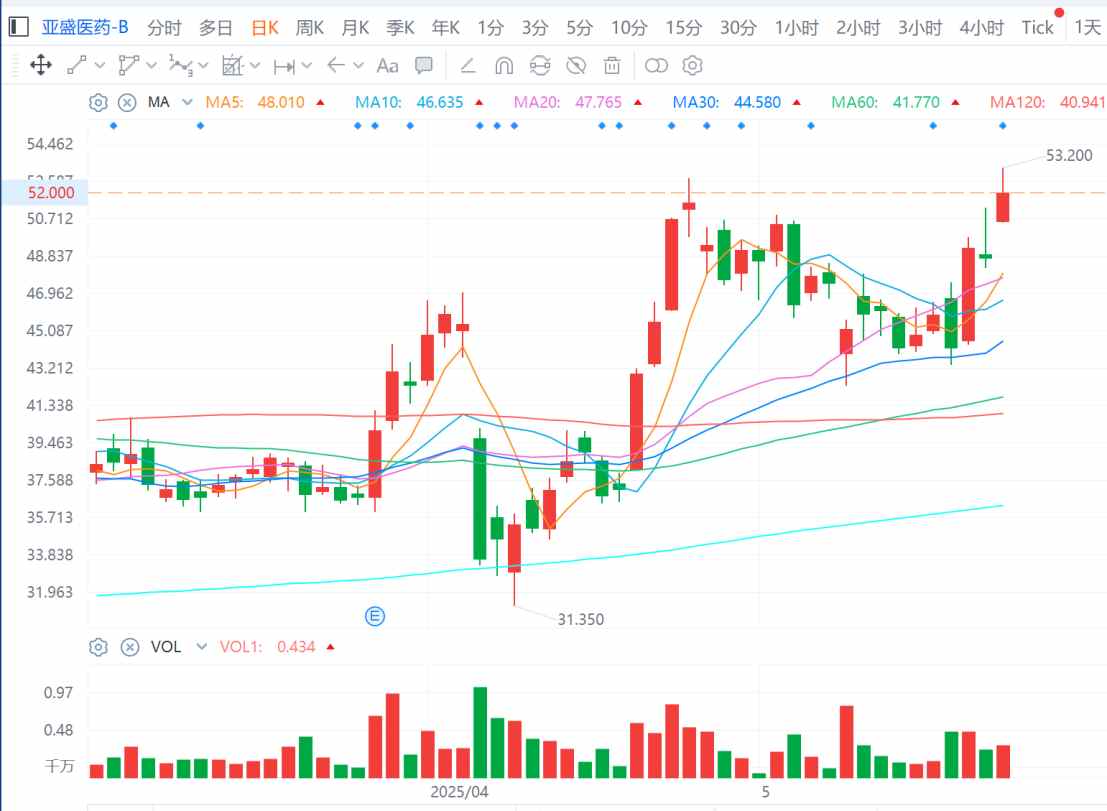
智通財經APP觀察到,早在5月23日,亞盛醫藥-B(06855)股價便高開高走,最高漲幅達到9.13%,股價最高觸及53.20港元,創下自2021年8月以來的新紀錄。二級市場之所以反應積極,在於當天盤前,公司披露了其在今年ASCO年會上的數據信息。
作為每年全球腫瘤學領域最前沿的臨床腫瘤學科研成果和腫瘤治療技術交流會議,美國臨床腫瘤學會(ASCO)年會從來不缺重磅的研究成果展示。而亞盛醫藥作為其常客,今年已在ASCO年會上分別以口頭報告和壁報形式公布APG-2575(Lisaftoclax)治療多種血液系統腫瘤和APG-115(Alrizomadlin)治療實體瘤的臨床研究最新進展。
Lisaftoclax best-in-class潛力進一步驗證
作為全球第二個遞交新藥上市申請(NDA)的Bcl-2抑制劑、中國首個遞交NDA並進入優先審評的國產原研Bcl-2抑制劑,Lisaftoclax(APG-2575)自I期臨床研發之初便高曝光於各大國際權威會議上,展現出了在多種血液腫瘤和實體瘤治療領域具備的廣闊治療前景,並獲得了全球業界的一致認可。
而在今年,Lisaftoclax又順利獲得獲2025版《CSCO淋巴瘤診療指南》推薦,用於單藥治療復發/難治性(R/R)慢性淋巴細胞白血病/小淋巴細胞淋巴瘤(CLL/SLL)患者。這是Lisaftoclax首次獲納入CSCO指南,並且是唯一獲得指南推薦的中國原研Bcl-2抑制劑。此次被納入CSCO指南,標誌着該藥物的循證證據獲得國內頂級學術機構認可。
在此背景下,Lisaftoclax最新研究成果以口頭報告形式亮相今年ASCO年會,無疑是全球業界關注的焦點。
據智通財經APP了解,此次Lisaftoclax口頭報告展示的研究為一項該品種聯合阿扎胞苷治療初治(TN)或既往接受過Venetoclax治療的髓系惡性腫瘤患者的Ib/II期臨床研究。此項全球多中心研究入組患者逾百人,數據顯示Lisaftoclax聯合阿扎胞苷的耐受性良好並已顯示初步療效。值得一提的是,該研究首次公布了Lisaftoclax在既往Venetoclax難治的急性髓系白血病(AML)患者及骨髓增生異常綜合徵(MDS)患者中的臨床數據,Lisaftoclax展示出克服Venetoclax耐藥的潛力,是國際上首次報告新型Bcl-2抑制劑克服Venetoclax耐藥的臨床研究。
數據表明,Lisaftoclax聯合阿扎胞苷的耐受性良好並已顯示初步療效截至2025年4月,共入組103例患者,其中包括新診斷和復發/難治的AML和MDS患者。
1. 在6例療效可評估的新診斷(ND)AML/混合表型急性白血病(MPAL)患者中,ORR為 83.3%, 其中33.3%的患者獲 CR/CRi ,50%的患者獲PR。在 44 例療效可評估R/R AML/MPAL 患者中,ORR為 43.2%,其中31.8% 的患者獲CR/CRi ,4.5%的患者獲PR,6.8% 的患者獲MLFS。
2.在15例療效可評估的 ND MDS/慢性粒單核細胞白血病(CMML)患者中,ORR為 80%,其中40%的患者獲CR,40%的患者獲骨髓CR(mCR)。22 例療效可評估的 R/R MDS/CMML 患者中,ORR為 50%,其中27.3%的患者獲 CR,18.2%的患者獲 mCR,4.5%的患者獲PR。
據智通財經APP了解,此次Lisaftoclax臨床試驗的患者對象初治(TN)或既往接受過Venetoclax(VEN)治療的髓系惡性腫瘤患者(Pts),因此Lisaftoclax在Venetoclax難治性患者中的療效表現,進一步驗證其best-in-class潛力。數據顯示,在28例既往Venetoclax耐藥的復發/難治 AML/混合表型急性白血病(MPAL)患者中,療效可評估的患者有22例,總反應率(ORR)為31.8%(7/22),其中22.8%的患者CR/ CR伴血細胞未完全恢復(Cri);4.6% 的患者獲部分緩解(PR);4.6%的患者獲形態學無白血病狀態(MLFS)。獲得治療反應的患者既往均接受過包括Venetoclax在內的多線治療,且大部分(71%,5/7)患者基線存在TP53突變並伴隨複雜染色體核型。
另外在安全性表現方面, Lisaftoclax聯合AZA治療,耐受性良好,安全性可控,常見不良反應主要體現在血液學事件,非血液學毒性不常見。絕大多數不良事件都可控制、可恢復、可耐受。
有望釋放20億美元銷售潛力
近日,三生製藥與輝瑞達成的一項總額高達60.5億美元的「出海」大單帶火了港股創新藥板塊,也讓全球業界和市場的目光再次聚焦於中國國產創新藥。
實際上,這只是國內創新藥行業飛速發展的一個縮影。近年來越來越多的真正具有創新能力、提供臨床價值、管線推進速度走在前列的國產創新藥企業開始脫穎而出,手握兩大「十億美元分子」潛力核心品種的亞盛醫藥便是其中之一。
此次Lisaftoclax最新臨床數據披露之所以值得全球業界和市場關注,在於相較國內Bcl-2抑制劑賽道的其他競爭者,先發優勢顯著。Lisaftoclax目前已進入上市倒計時,作為未來1-2年內亞盛醫藥最大的基本面催化劑事件之一,這將是亞盛醫藥又一個重要的質變時刻。
從市場角度來看,以CLL/SLL適應症為例,作為成人白血病最常見的類型,CLL/SLL佔西方國家白血病病例的四分之一,全球每年新增病例超過10萬例。儘管當前的一線治療,如免疫療法、化療和BTK抑制劑對初治患者有顯著反應,但復發和耐藥是主要的臨床挑戰。CLL/SLL的治療中仍存在着顯著的、未滿足的臨床需求,迫切需要新的治療選擇。
雖然Bcl-2抑制劑的出現讓CLL/SLL的治療有了進一步的革新。然而BCL-2靶點研發門檻較高。由於BCL-2靶點結合的界面比較大及跨線粒體膜運輸問題,導致該靶點成藥設計十分艱難。BCL-2靶點發現至今40年,目前全球獲批上市的Bcl-2抑制劑也僅有艾伯維的Venetoclax,充分展現了該領域的研發難度與挑戰。
當前,國外的CLL/SLL臨床治療已進入了「無化療」「固定療程」的新時代,而美國國家綜合癌症網絡(NCCN)指南也將Bcl-2抑制劑推薦為BTKi治療失敗的CLL/SLL患者的治療首選。
2024年全球血液惡性腫瘤治療藥物市場規模達400億美元,2024-2029年CAGR增長達6%。以目前全球唯一一款獲批上市的Bcl-2抑制劑Venetoclax為例,其2024年銷售額達25.83億美元,按年增長12.66%,足以從側面看出全球市場對Bcl-2抑制劑的龐大未滿足需求。
此前Lisaftoclax披露的臨床數據已經驗證了其在CLL/SLL患者中具備單藥和聯合治療的BIC潛力,而此次Lisaftoclax在ASCO年會上披露的最新臨床數據,則進一步驗證了其在Venetoclax臨床失敗的適應症上的良好治療效果和成藥預期,為其上市後的市場增長確定性再添上一枚關鍵的砝碼。
參考Venetoclax市場表現,Lisaftoclax上市後銷售超20億美元的確定性正逐漸增強。並且,如今Lisaftoclax還展現出了在克服Venetoclax耐藥方面的巨大潛力,隨着後續在MM、MDS領域持續突破,其未來峯值銷量有望超越Venetoclax。
結語
一直以來,亞盛醫藥Lisaftoclax受到全球業界廣泛關注的關鍵原因在於,此前多項臨床數據驗證其安全性優勢更加突出,且在多種血液腫瘤治療領域具備廣闊的治療前景,特別在CLL/SLL患者中具有單藥和聯合治療潛力。
而此次針對Venetoclax難治性患者的治療數據披露,Lisaftoclax憑藉其優異的臨床數據,進一步鞏固了其Best-in-Class潛力屬性。
作為全球第二個遞交新藥上市申請(NDA)的Bcl-2抑制劑、中國首個遞交NDA並進入優先審評的國產原研Bcl-2抑制劑,Lisaftoclax目前在商業化進度上已領先於全球其他在研的Bcl-2抑制劑,未來在更佳的臨床表現加持下,邁向商業化階段的的Lisaftoclax有望成為亞盛醫藥下一個「十億美元分子」,成為引爆亞盛醫藥估值增長的下一個重磅炸彈。