得益於政策利好及醫保支付邊際改善等因素,近期港股創新藥板塊熱度持續居高不下,多隻港股醫藥ETF年內漲幅超過40%,領跑同類產品。5月29日,國家藥品監督管理局一天內集中批准了11款創新藥上市,標誌着中國創新藥行業已進入集中上市期。
在創新藥板塊受到多方關注之際,一家創新藥企業赴港IPO可謂「恰逢其時」。據港交所公開文件披露,贛州和美藥業股份有限公司(簡稱 「和美藥業」)向港交所主板遞交上市申請,國證國際為其獨家保薦人,投資方包括真灼投資、上海鴻富、君聯資本、泰格醫藥、倚鋒資本等。
公開資料顯示,和美藥業成立於2002年,是一家創新驅動的生物製藥公司,致力於發現和開發針對自身免疫性疾病和腫瘤的小分子藥物,並在銀屑病、白塞病和炎症性腸病和創新化學療法開發中處於行業前沿地位。目前和美藥業已經完成了6輪孖展,最新一輪投後估值39億元。
截至最新財務報告,和美藥業仍未實現盈利,於2023年度及2024年度,公司收益分別約為405萬元、529.8萬元(單位為人民幣,下同),主要來自政府補助,同期年內虧損則分別約為1.56億元、1.23億元。
如和美藥業這般以18A規則上市的生物醫藥企業通常具有高投入、高產出的特點,候選藥物的商業化前景將成為影響企業長期估值水平的重要因素。和美藥業此次上市是否能贏得市場青睞,還是需要從其研發管線來看。
銀屑病新藥能否從激烈競爭中「突圍」?
對於一家創新藥企,衡量其未來成長潛力的關鍵就在於其研發管線。
智通財經APP了解到,截至最新披露日,和美藥業已開發七個小分子候選藥物,針對具有高度未滿足需求的自身免疫和腫瘤疾病。截至2025年5月21日,其中四種處於II期、III期臨牀試驗或NDA階段,適用於12種適應症。
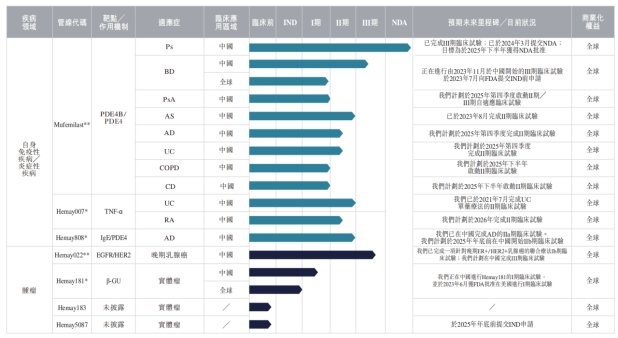
和美藥業共擁有兩款核心產品,有望成為全球首創銀屑病治療藥物的Mufemilast和EGFR/HER2雙靶點抗癌藥Hemay022。
其中,Mufemilast是一種新型小分子磷酸二酯酶4B(PDE4B)蛋白表達阻斷劑和PDE4抑制劑,具有廣泛的自身免疫性疾病治療潛力。其不會引起血管炎,也不會輕易穿過血腦屏障,從而減少了中樞神經系統副作用,如抑鬱和自殺傾向。截至2025年5月21日,Mufemilast也是唯一可直接用於有潛伏性結核感染的銀屑病(Ps)患者的藥物,其安全性獲III期臨牀試驗支持。
截至2025年5月21日,公司已於中國完成Mufemilast作為單一療法治療Ps的關鍵性III期臨牀試驗,且於2024年3月就Mufemilast作為Ps治療提交的NDA正在接受優先審評;正在進行白塞病(BD)的關鍵性III期臨牀試驗;已完成強直性脊柱炎(AS)的II期臨牀試驗。
此外,就克羅恩病及慢性阻塞性肺病而言,公司正計劃在中國開展II期臨牀試驗,預期將於2025年下半年開始招募首批患者;潰瘍性結腸炎(UC)和特應性皮炎(AD)的非關鍵性II期臨牀試驗正在進行中。
而談到Mufemilast的商業化前景,其進展最快的適應症為銀屑病,這是一種常見於膝蓋、肘部、頸部和頭皮的皮膚病,是一種自身免疫性疾病。吸菸率的上升、生活方式的改變、飲酒量的增加等因素都可能導致各年齡段人羣中銀屑病發病率增加。數據顯示,2024年,全球銀屑病藥物市場規模為296.21億美元,預計在2024-2029年預測期內該市場將以9.19%的複合年增長率增長。
智通財經APP了解到,目前全球銀屑病藥物按治療類型分為局部用藥、系統療法和生物製劑。隨着對銀屑病發病機制認識的深入,近年來各種生物製劑、小分子靶向藥和外用藥相繼湧現。
而在生物製劑中,銀屑病藥物可主要分為白細胞介素(IL)抑制劑、腫瘤壞死因子α(TNF-α)抑制劑和磷酸二酯酶4(PDE-4)抑制劑等,其中Mufemilast就屬於PDE-4抑制劑。但相比於傳統的PDE-4抑制劑,Mufemilast具有PDE4B蛋白表達阻斷劑和PDE4抑制劑的雙重機制,與單獨使用PDE4抑制劑相比,潛在副作用較低,治療效果也較好。
在PDE-4抑制劑這一賽道,全球市場上已有由美國安進公司(Amgen)生產的全球首個口服PDE-4抑制劑阿普米斯特片,該藥堪稱銀屑病治療領域的革命性藥物。自2014年3月獲FDA批准上市以來,阿普米司特片的適應症不斷擴展,先後用於治療活動性銀屑病關節炎、光療和系統療法中的中度至重度斑塊型銀屑病,早在2022年其全球銷售額就已達到22.88億美元。
在國內,2025年4月阿普米司特片已通過第十批國家集採,資料顯示,該批集採藥物價格平均降幅超60%。此外,截至目前,已有十餘家企業研發的阿普米司特仿製藥在國內成功上市,如齊魯製藥、正大清江製藥等都有相關上市產品。

(圖:阿普米司特片中選結果)
儘管Mufemilast相對於傳統PDE-4抑制劑有一定優勢,但在國內市場,各種各樣的銀屑病新藥仍然層出不窮,如三生國健、信達生物都已有銀屑病新藥上市申請獲得CDE受理。在現有市場競爭已經相當激烈的情況下,Mufemilast即使成功上市也將面臨「前有狼後有虎」的困難境地,其商業化前景仍屬於未知之數。
和美藥業的另一款核心產品Hemay022是一種新型EGFR/HER2雙靶點小分子抑制劑,旨在治療晚期乳腺癌。Hemay022與芳香化酶抑制劑聯合使用時,通過抑制HER2和EGFR的異常激活發揮其抗腫瘤作用,同時減少雌激素分泌。此外,在ER+/HER2+乳腺癌患者中,Hemay022聯合內分泌治療有助於推遲獲得性耐藥的發生。截至2025年5月21日,公司正在進行一項針對晚期ER+/HER2+乳腺癌的III期聯合療法臨牀試驗。
作為蛋白酪氨酸激酶家族成員,表皮生長因子受體(EGFR)和人表皮生長因子受體2(HER2)在細胞信號轉導中發揮核心作用,這兩種受體的過表達或異常活化與多種實體瘤發生密切相關,已成為抗癌藥物開發的重要靶點。
目前全球範圍內已有多個EGFR/HER2雙抑制劑進入臨牀階段,如德國勃林格殷格翰公司開發生產的第二代不可逆EGFR/HER2抑制劑阿法替尼,對罕見EGFR突變有很好的療效,能控制和預防腦轉移,且對肺鱗癌也有一定的治療作用;尼妥珠單抗(nimotuzumab)、甲苯磺酸拉帕替尼(Lapatinib Ditosylate)、莫博賽替尼(mobocertinib)等EGFR/HER2雙抑制劑也已早早獲批上市,Hemay022未來的競爭壓力同樣不容小覷。
此外,和美藥業管線中還有多項研發中產品,如TNF-α小分子調節劑Hemay007,已完成單藥治療UC的II期臨牀試驗,正在進行RA的II期臨牀試驗;靶向IgE和PDE4的新型分子實體Hemay808,已於中國完成治療AD的IIa期臨牀試驗,計劃在2025年年底於中國啓動IIb期臨牀試驗;一種潛在同類首創且具有專有作用機制的拓撲異構酶I靶點SDC藥物Hemay181,具有廣譜抗腫瘤潛力,已於2023年6月獲FDA批准在美國進行I期臨牀試驗,正在於中國進行I期臨牀試驗。
多項研發中產品將為公司帶來不小的資金壓力,2023-2024年,公司研發投入分別為1.23億元和0.97億元,截至2024年12月31日公司持有現金和現金等價物約1.5億元,高額的研發開支導致公司財務狀況較為緊張,這或許也是和美藥業急於上市的原因之一。
小結
整體來看,儘管公司核心產品銀屑病新藥進展較快,但該賽道已存在多款已上市和即將上市藥物,激烈的市場競爭或顯著擠壓其商業化空間。與此同時,多項在研管線仍處高投入階段,將持續對公司財務狀況形成壓力。在商業化前景尚存不確定性的情況下,和美藥業想要贏得資本市場青睞恐非易事。