炒股就看金麒麟分析師研報,權威,專業,及時,全面,助您挖掘潛力主題機會!
IT之家 7 月 13 日消息,復旦大學上海醫學院彭勃、饒豔霞團隊與上海交通大學曹立團隊(兼上海市第六人民醫院團隊)合作。
該研究首次證實通過替換中樞神經系統中的致病性小膠質細胞,成功阻斷致命成人起病軸突膨脹伴色素膠質細胞腦白質病(ALSP)的病程進展,並首次在人類 ALSP患者中系統性驗證了小膠質細胞替換策略的臨床可行性與長期療效。
據官方介紹,患者在治療後長達 24 個月的隨訪期間,疾病進展停止,運動功能得以保留,且認知能力保持穩定。
相關成果已於 7 月 11 日發布在《科學》(Science)上(IT之家附 DOI: 10.1126/science.adr1015)。

小膠質細胞(Microglia)是中樞神經系統(CNS)中重要的免疫細胞。小膠質細胞功能障礙會導致多種中樞神經系統疾病。CSF1R主要在小膠質細胞中表達,對小膠質細胞的存活和功能至關重要。CSF1R 的雙等位基因突變會導致先天性小膠質細胞缺失,並在人類和小鼠中均造成圍產期死亡,而單等位基因突變則會導致 CSF1R 相關的小膠質細胞病(CAMP),這是成人起病軸突膨脹伴色素膠質細胞腦白質病(ALSP)的主要形式。
ALSP 是一種由 CSF1R 基因突變引發的遺傳性神經退行性疾病,患者成年後發病,平均生存期僅 3-6.8 年左右。突變導致小膠質細胞功能異常,數量銳減且從「大腦保衛者」變為「破壞者」,引發腦白質脫髓鞘、軸突腫脹、認知與運動功能退化,最終導致神經功能喪失。
在我國,ALSP 患者在發病後的平均生存期僅為3年,全球目前尚無明確有效的根治或緩解方法,患者往往在病情進展中喪失自理能力,生存質量極差。
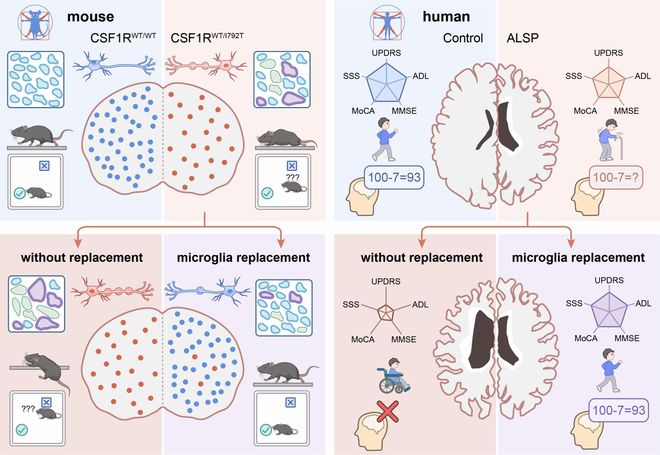 ▲基於小膠質細胞替換的細胞治療策略
▲基於小膠質細胞替換的細胞治療策略該研究不僅在動物模型中實現超 90% 的小膠質細胞高效替換,更在 8 例 ALSP 患者中完成兩年隨訪,證明傳統骨髓細胞移植(tBMT)可通過機制創新實現小膠質細胞替換,阻止患者病情惡化。標誌着我國在小膠質細胞替換領域的國際領先地位。
實際上,彭勃團隊早在 2020 年就首次提出「小膠質細胞替換策略」,這一顛覆傳統的「細胞乾坤大挪移」創新療法開發出三種路徑:
該策略也被簡稱為MISTER(通過替換進行的小膠質細胞干預治療和增強策略),該策略此後為該領域的後續研究提供了信息和啓發。研究團隊推斷,該策略對於 ALSP 具有治療潛力。
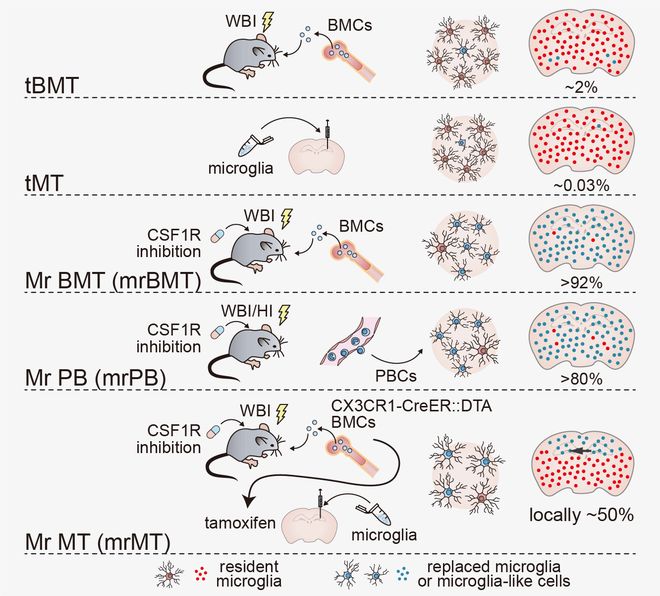 ▲全球首次實現的小膠質細胞替換策略
▲全球首次實現的小膠質細胞替換策略研究首次完成了模擬人類 ALSP 病理的關鍵動物模型構建。傳統 ALSP 動物模型(如 CSF1RWT / KO 或 CSF1R-ΔFIRE 小鼠)無法真實再現患者「小膠質細胞數量減少但未消失」的病理特徵,在一定程度上制約了研究進展。團隊基於全球患者突變譜,建立攜帶 CSF1R 基因熱點突變(分別對應於小鼠的 I792T 和 E631K 突變)的小鼠模型,首次全面復現 ALSP 的病理學和行為學特徵,為機制研究和療效驗證提供可靠工具。
為了驗證臨床相關性,研究團隊在 8 名 ALSP 患者中進行了基於 tBMT 的小膠質細胞替換治療。通過使用非侵入性的正電子發射斷層掃描(PET)成像技術,研究團隊發現,腦部葡萄糖代謝增加。
值得注意的是,在長達 24 個月的隨訪期間,磁共振成像(MRI)和臨床評估顯示,患者的疾病進展停止,運動功能得以保留,認知能力保持穩定。
該研究還為之前的一個臨床病例提供了機制解釋,該病例中一名最初被誤診為成人發病型異染性腦白質營養不良的 ALSP 患者在接受 tBMT 治療後,實現了長期病情穩定。這也是首次在人類患者中系統性驗證小膠質細胞替換策略的臨床可行性與長期療效。
(轉自:網易科技)