炒股就看金麒麟分析師研報,權威,專業,及時,全面,助您挖掘潛力主題機會!
(來源:虎嗅APP)

本文來自微信公衆號:和觀醫療,作者:和光觀察,原文標題:《創新藥洞察(一):CAR-T 企業的支付突圍與價值解析》《創新藥洞察(二):9 家 CAR-T 企業技術路線 PK,誰能率先把成本砍半?》,題圖來自:AI生成
當醫藥研發進入「第四代革命」,細胞治療(尤其是 CAR-T 療法)正以顛覆性力量重塑癌症治療格局——它不再是實驗室裏的概念,而是實實在在讓復發 / 難治的腫瘤患者實現長期緩解的「活藥物」。
與此同時,港股生物創新藥板塊持續成為國內外資本關注的焦點,2024 年以來,細胞治療領域的 BD 交易金額突破 50 億美元,一批中國創新藥企通過自主研發與國際合作,正從「追隨者」向「領跑者」躍遷。
國內創新藥的發展已駛入快車道:從靶點創新到技術突破,從臨床數據驚豔到商業化落地,一系列 BD 項目(如授權合作、聯合開發)凸顯了創新藥企即將開啓的「價值創造時代」。但機遇背後,風險與挑戰並存:誰能在這場細胞治療浪潮中佔領潮頭? 答案不僅取決於技術領先性,更依賴對臨床數據、技術迭代、成本控制、市場準入與政策環境的綜合判斷。
正基於此,筆者在前著的《首年商保創新藥目錄:CAR-T談判的核心關注點解析》之後,繼續深度分析——聚焦中國 CAR-T 研發的 9 家企業,拆解技術、成本、市場準入與支付、出海的底層邏輯,為關注港股生物藥及醫藥創新 BD 的投資者提供參考。
當前 CAR-T 市場正面臨關鍵矛盾:療效顯著但價格高昂,患者需求迫切但支付能力有限,這也是未來能否實現規模化普及的核心破局點。
從價格端看,已上市的 CAR-T 產品單療程費用普遍在百萬元,如合源生物(納基奧侖賽)的99.9 萬元、藥明巨諾(瑞基奧侖賽的129 萬元),遠超普通患者的支付能力。從需求端看,以復發/難治性多發性骨髓瘤為例,中國年新發病例約 2.5 萬人[1,4,14],非霍奇金淋巴瘤年新發病例約 6 萬[2,7,8],這些患者對 CAR-T 療法有強烈需求,但高昂價格讓多數人望而卻步。
付體系成為關鍵變量:短期內,商業健康保險是主要支撐,但目前僅有42%(78款[15])的惠民保保障方案中明確將 CAR-T 納入報銷,且非既往症患者賠付比例均值為71%[15],既往症患者賠付均值則僅為32%[15],保障水平有限;
中長期看,只有當價格降至 30 萬元以下,基本醫保纔可能納入,實現「以價換量」。因此,企業能否通過技術迭代降低成本、通過適應症擴展擴大患者規模,直接決定了在「量價博弈」中的勝負。
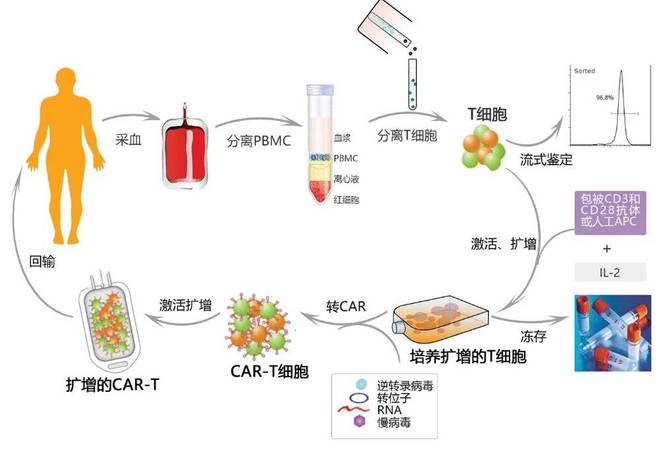
CAR-T 價格昂貴的本質是「個性化+高技術壁壘」的生產模式。但技術迭代正在打開成本下降空間,核心影響因素包括:
1. 載體技術:從「病毒依賴」到「非病毒突破」
傳統 CAR-T 依賴慢病毒 / 逆轉錄病毒載體,生產周期長(2—4 周)、成本高(佔總成本 30%—50%)[16]。非病毒載體(如 mRNA-LNP、電穿孔)無需病毒培養,可將載體成本降低 30%—50%[17][18],目前科濟製藥、藥明巨諾等企業已佈局相關技術。
2. 自體vs異體:從「一人一藥」到「批量生產」
自體 CAR-T 需為每位患者單獨製備,無法規模化;異體 CAR-T(通用型)可從健康供體提取 T 細胞批量改造,單患者成本可降至自體的 1/3—1/2[19,20]。科濟製藥的 THANK-uCAR®、合源生物的 HY035 等通用型平台已進入臨床前 / 早期臨床,是中長期降本關鍵。
3. 生產工藝:從「人工操作」到「自動化提速」
傳統生產依賴人工操作,耗時 14 天以上;自動化封閉系統(如科濟製藥 CARcelerate® 平台)可將製備時間縮短至 30 小時,減少人力與試劑消耗,直接降低成本 40% 以上[21,22,23]。
為系統性解析 CAR-T 投資機會,系列文章將從多個核心維度層層深入,最終對 9 家企業的投資潛力進行總結。
1. 技術迭代與成本控制
追蹤 9 家企業的核心技術路線(自體 / 異體、病毒 / 非病毒載體等),評估中長期成本下降趨勢與潛力。
2. 研發管線佈局與市場潛力
結合流行病學數據,測算各研發管線,在研產品的適應症(如血液腫瘤、實體癌等)的潛在患者規模,判斷各家企業CAR-T產品中長期的市場潛力規模。
3. 藥物經濟學與市場準入
在國內創新藥醫保談判與商業健康險補充的背景下,誰家CAR-T產品更有機會取得市場準入的優勢?即基於製備成本控制能力,及研發管線的市場潛力分析,預判二者疊加形成的「成本-患者量」 雙優勢企業,誰更可能在商保談判中更有優勢取得「量價協議」,甚至進入基本醫保談判的可能。
4. 出海機會與國際化能力
從海外臨床同步性、技術自主性、國際合作等角度,評估產品在歐美 / 新興市場的拓展潛力。
5. 商業化能力與投資關係
關注已上市產品銷售額、產能、渠道佈局,以及投資關係對研發的支撐能力,規避商業化風險。
系列分析聚焦的9 家 CAR-T 企業,均來自 NMPA/CDE 的臨床研究與上市申請數據庫,是中國 CAR-T 研發的「第一梯隊」——包括已獲批上市6款CAR-T產品(如傳奇生物西達基奧侖賽、復星凱特阿基侖賽),5個進入關鍵臨床 / 上市申請階段(如科濟製藥澤沃基奧侖賽),以及這9家企業的在研的CAR-T 管線中產品。
CAR-T 療法在癌症治療領域的巨大潛力,但其百萬的價格與有限的保險支付形成了尖銳矛盾,嚴重阻礙了其廣泛普及。目前 CAR-T 的高成本源於其個性化定製的模式,為每位患者單獨製備細胞,使得成本難以分攤。未來,哪家企業能借助技術迭代,顯著降低成本,無疑將在市場準入的激烈競爭中搶佔先機,贏得競爭優勢,這也是投資者判斷企業投資價值潛力的關鍵所在。
1. 細胞來源:自體CAR-T vs異體(通用型)CAR-T
自體CAR-T:從患者自身外周血採集T細胞,經基因修飾後回輸。這種「個體化定製」的方式安全性高,幾乎無免疫排斥風險,臨床驗證也較為成熟,已上市的阿基侖賽、瑞基奧侖賽等均屬此類。不過,其製備周期長達2—4周,成本極高,單劑成本常超百萬,且約10%—20%的患者因自身T細胞質量問題無法制備合格產品。
異體(通用型)CAR-T:從健康捐贈者的T 細胞採集、批量修飾,可多次用於不同患者。它能實現批量生產,製備時間大幅縮短至 1—3 天[1],成本有望降低50%—70%[2,3,4,5]。但面臨免疫排斥難題,需通過基因編輯敲除相關基因,技術難度高,長期安全性也有待驗證。
2. 基因轉導載體:病毒載體vs非病毒載體
病毒載體:利用改造後的無致病性病毒作為「運輸車」,將CAR基因導入T細胞,常用慢病毒、逆轉錄病毒。其轉導效率高,可達70%—90%[7],CAR蛋白表達持久。但生產複雜,成本高,單批次生產成本佔CAR-T 總費用的30%—50%[6,8],還存在 「插入突變」[9]風險。已上市的多數CAR-T 產品採用慢病毒載體。
非病毒載體:通過物理或化學方法,如mRNA、轉座子、電穿孔等將 CAR 基因導入T 細胞。安全性高,無病毒整合風險,成本僅為病毒載體的 1/10—1/5[10]。然而,轉導效率較低,僅 30%—60%,且 CAR 蛋白表達短暫。
3. 細胞修飾方式:傳統CAR-T vs 基因編輯增強型CAR-T
傳統 CAR-T:僅導入 CAR 基因,不改變 T 細胞其他基因,技術成熟、研發周期短。但 T 細胞易被腫瘤微環境抑制,還可能引發嚴重細胞因子風暴,發生率可達 30%—50%[11]。
基因編輯增強型 CAR-T:在導入 CAR 基因的同時,通過 CRISPR/Cas9 等工具敲除 「抑制 T 細胞功能的基因」,或插入 「增強功能的基因」 (如細胞因子 IL-15)。可增強抗腫瘤活性(客觀緩解率提升 20%—30%)、降低 CRS 發生率(從 30%—50% 降至 10%—15%)[12]。不過,技術複雜度高,CRISPR/Cas9 脫靶風險約為 0.1%—1%[13],研發周期較傳統技術增加 30%—50%[14,15]。
4. 未來技術路線方向展望與成本影響總結
異體技術普及:中期(2025—2028 年),隨着異體 CAR-T 技術的臨床推進,單患者成本有望降低至 4 星;長期(2028 年後)結合非病毒載體等技術,成本可能進一步下降至 3 星[16]。
非病毒載體替代:採用 mRNA-LNP 或電穿孔等非病毒載體技術,可省去病毒培養環節,預計成本降低 30%—50%[17,18,19,20]。
(按企業名稱排序,1—5 星,星數越多成本越高)
1. 科濟藥業
短期(2025 年,目前階段)
技術路線:自體 + 慢病毒載體(澤沃基奧侖賽獲批實體瘤適應症,個性化製備)
成本評估:★★★★★(單劑成本超百萬,依賴個性化生產)[21]
中期(2025—2028 年)
技術路線:異體 + 病毒載體(THANK-uCAR® 通用型平台進入 II 期臨床,基因編輯敲除 NKG2A)
成本評估:★★★★☆(批量生產降低單劑成本,預計較短期下降 30%—40%)[22]
長期(2028 年後)
技術路線:異體 + 非病毒載體(mRNA-LNP 遞送技術落地,實現規模化生產)
成本評估:★★★☆☆(非病毒載體省去病毒培養環節,預計成本較中期再降 30%—50%)[7,20]
2. 合源生物
短期(2025 年,目前階段)
技術路線:自體 + 慢病毒載體(納基奧侖賽針對 B-ALL,生產成功率 100%)
成本評估:★★★★★(依賴慢病毒載體和個性化生產,成本維持高位)[23]
中期(2025—2028 年)
技術路線:異體 + 病毒載體(HY035 通用型平台完成臨床前研究,消除 HLA 匹配問題)
成本評估:★★★★☆(批量生產模式初步落地,成本較短期下降 25%—35%)[24]
長期(2028 年後)
技術路線:異體 + 非病毒載體(電穿孔技術替代病毒載體,優化生產流程)
成本評估:★★★☆☆(非病毒載體 + 自動化生產,預計成本較中期下降 40% 以上)[25,26,27]
3. 藥明巨諾
短期(2025 年,目前階段)
技術路線:自體 + 慢病毒載體(瑞基奧侖賽優化懸浮培養技術,生產成本降低 40%)
成本評估:★★★★☆(工藝優化使成本略低於同類自體產品)[28]
中期(2025—2028 年)
技術路線:自體 + 非病毒載體(引入 Juno 電穿孔技術,降低載體成本 30%)[29]
成本評估:★★★★☆(非病毒載體初步替代病毒,但自體模式仍限制降本空間)
長期(2028 年後)
技術路線:自體 + 非病毒載體(非病毒遞送技術成熟,自動化系統全面應用)
成本評估:★★★☆☆(非病毒載體 + 全自動化生產,單劑成本有望降至 30 萬元以下)[8,30,31]
4. 傳奇生物
短期(2025 年,目前階段)
技術路線:自體 + 慢病毒載體(西達基奧侖賽全球獲批,雙 BCMA 靶點設計)
成本評估:★★★★★(個性化生產 + 慢病毒載體,成本維持行業平均水平)[32]
中期(2025—2028 年)
技術路線:自體→異體 + 病毒載體(與楊森合作開發異體平台,探索雙靶點設計)
成本評估:★★★★☆(逐步過渡至異體模式,批量生產降低部分成本)[33]
長期(2028 年後)
技術路線:異體 + 非病毒載體(非病毒遞送技術與異體平台結合,實現規模化)
成本評估:★★★☆☆(異體批量生產 + 非病毒載體,預計成本較中期下降 40%—50%)[34,35,36]
5. 馴鹿生物
短期(2025 年,目前階段)
技術路線:自體 + 慢病毒載體(伊基奧侖賽為雙靶點 BCMA/CD19 CAR-T,慢病毒轉染)
成本評估:★★★★★(雙靶點設計增加工藝複雜度,成本略高於單靶點產品)[37]
中期(2025—2028 年)
技術路線:雙特異性 + 病毒載體(擴展至實體瘤適應症,優化慢病毒轉染效率)
成本評估:★★★★★(仍依賴病毒載體和自體生產,成本下降有限)[38]
長期(2028 年後)
技術路線:雙特異性 + 非病毒載體(mRNA 遞送技術提升實體瘤穿透性,降低載體成本)
成本評估:★★★☆☆(非病毒載體替代病毒,預計成本較中期下降 40%—50%)[39,40,41]
6. 復星凱瑞
短期(2025 年,目前階段)
技術路線:自體 + 逆轉錄病毒載體(阿基侖賽引入 Kite 技術,依賴個性化生產)
成本評估:★★★★★(國內首款上市 CAR-T,技術授權成本疊加個性化生產,成本高位)[42]
中期(2025—2028 年)
技術路線:雙特異性 + 病毒載體(CD19/CD22 雙靶點進入 II 期,引入 Kite 異體技術儲備)
成本評估:★★★★★(雙靶點工藝複雜,異體技術尚未落地,成本維持高位)[43]
長期(2028 年後)
技術路線:雙特異性 + 非病毒載體(非病毒遞送實現通用型生產)
成本評估:★★★☆☆(非病毒載體 + 通用型模式,預計成本較中期下降 50% 以上)[44,45,46]
7. 永泰生物
短期(2025 年,目前階段)
技術路線:自體 + 病毒載體(迪諾侖賽靶向 TGF-β 信號阻斷,公開技術細節有限)
成本評估:★★★★★(基於現有報道推測,依賴自體生產和病毒載體,成本高位)[47]
中期(2025—2028 年)
技術路線:自體 + 病毒載體(TGF-β 阻斷技術擴展至實體瘤,未披露異體或非病毒佈局)
成本評估:★★★★★(暫時缺少詳細技術迭代信息,基於現有數據推測成本下降有限)[48]
長期(2028 年後)
技術路線:未明確披露(未公開通用型或非病毒載體研發計劃)
成本評估:★★★★★(基於現有報道推測,若技術路線無重大突破,成本難以下降)[49,50,51]
8. 恒潤達生
短期(2025 年,目前階段)
技術路線:自體 + 慢病毒載體(CD19/CD20 雙靶點 CAR-T,工藝優化信息有限)
成本評估:★★★★★(基於現有數據推測,雙靶點 + 自體生產,成本維持高位)[52]
中期(2025—2028 年)
技術路線:自體 + 病毒載體(CD19/CD20 雙靶點推進至 II 期,未披露新技術佈局)
成本評估:★★★★★(暫時缺少詳細降本技術信息,推測成本下降幅度低於 20%)[53]
長期(2028 年後)
技術路線:未明確披露(未公開通用型或非病毒載體研發動態)
成本評估:★★★★☆(基於現有報道推測,若工藝優化落地,成本或小幅下降 10%—20%)[54,55,56]
9. 重慶精準生物
短期(2025 年,目前階段)
技術路線:自體 + 慢病毒載體(普基侖賽為 CD19/CD22 雙靶點,生產模式未公開)
成本評估:★★★★★(基於行業同類產品推測,自體 + 病毒載體成本高位)[57]
中期(2025—2028 年)
技術路線:自體 + 病毒載體(探索實體瘤適應症,未披露技術迭代計劃)
成本評估:★★★★★(暫時缺少詳細研發動態,推測成本維持高位)[58]
長期(2028 年後)
技術路線:未明確披露(無公開信息顯示佈局通用型或非病毒技術)
成本評估:★★★★★(基於現有數據推測,技術路線無突破則成本難以下降)[50,60]
10. 技術路線對企業CAR-T成本的影響總結
明確降本路徑的企業:科濟藥業、合源生物、藥明巨諾通過 「異體 + 非病毒」 雙路徑佈局,短期依賴工藝優化,中長期藉助技術迭代實現成本大幅下降,長期成本有望降至 3 星及以下。
技術轉型中的企業:傳奇生物、馴鹿生物、復星凱特短期仍依賴自體 + 病毒載體,但長期規劃包含非病毒或異體技術,成本下降潛力取決於技術落地速度。
信息有限的企業:永泰生物、恒潤達生、重慶精準生物目前公開的技術迭代信息較少,短期至長期成本評估基於現有數據推測,未來若有技術突破可能改變成本趨勢,但存在較高不確定性。




說明:本文對 9 家 CAR-T 企業技術路線及成本的評估,均基於目前已公開的信息、行業研究及數據推測得出。由於 CAR-T 技術研發具有高風險性,企業的技術路線推進、成本控制效果等均可能受到臨床進展、技術突破難度、政策環境等多種因素影響,未來發展存在較大不確定性。因此,本文的評估結果僅供參考,不構成任何投資建議。投資者及相關人士需持續關注企業動態及行業變化,以便做出更準確的判斷。
本文來自微信公衆號:和觀醫療,作者:和光觀察,原文標題:《創新藥洞察(一):CAR-T 企業的支付突圍與價值解析》《創新藥洞察(二):9 家 CAR-T 企業技術路線 PK,誰能率先把成本砍半?》
本內容為作者獨立觀點,不代表虎嗅立場。未經允許不得轉載,授權事宜請聯繫 hezuo@huxiu.com
本文來自虎嗅,原文鏈接:https://www.huxiu.com/article/4647951.html?f=wyxwapp