紅星資本局10月19日消息,10月17日晚,福建海西新藥創制股份有限公司(下稱「海西新藥」)在港交所發布公告稱,將於10月20日(星期一)正式上市,發售價格為86.40港元/股。
海西新藥原定於10月17日在港股正式掛牌交易。作為2023年FINI制度(指香港2023年11月推行的新股發行制度改革)落地以來,首隻在暗盤交易結束後因未能刊發配髮結果而延遲上市的新股,海西新藥暗盤交易是否會取消等問題此前一度引發市場關注。
紅星資本局諮詢相關券商人工客服獲悉,若投資者暗盤交易已經成交,即證明已經賣出,交易不會作廢。此外,在社交平台上,已有不少網友曬圖顯示賣出金額已到賬。
10月19日,紅星資本局就上市事宜致電海西新藥投資者熱線,電話未獲接通。
紅星資本局注意到,與其他以18A章規則(指2018年港交所推出上市規則第18A章後,在港股上市的未盈利生物科技企業)尋求港股上市的創新藥企業不同,海西新藥已有15款仿製藥獲批上市,靠4款核心仿製藥年入超4億元,並有4款創新藥在研。
銷售團隊僅36人
靠4款核心仿製藥年入超4億元
資料顯示,海西新藥於2012年3月在福州成立,是一家通過仿製藥盈利的製藥公司。截至招股書披露日,海西新藥獲批上市的仿製藥產品有15款,產品組合涵蓋了多個治療領域,包括消化系統、心血管系統、內分泌系統、神經系統等。
招股書顯示,2022年至2024年,海西新藥營收從2.12億元增長至4.67億元,淨利潤從6898萬元增長至1.36億元。2025年前五個月,海西新藥實現營收2.49億元,淨利潤9021萬元。
從產品結構來看,公司的營收主要依賴安必力(枸櫞酸莫沙必利片)、海慧通(氨氯地平阿託伐他汀鈣片)這兩款產品,營收佔比在70%以上。
其中,海慧通於2022年1月上市,用於治療高血壓、冠心病及高膽固醇血癥,2024年為公司貢獻1.87億元收入,在全國以59.3%的市場份額在其產品類別中排名第一。安必力於2020年6月上市,主要用於治療功能性消化不良,是同類首款通過仿製藥一致性評價的產品。2024年,安必力為公司貢獻了1.46億元收入,在全國以25.7%的市場份額在其產品類別中排名第二。
2021年以來,安必力、瑞安妥(鹽酸西那卡塞片)、海慧通、賽西福(硫酸羥氯喹片)相繼入選國家VBP(國家藥品集中採購)計劃。從2024年的營收情況看,這4款核心仿製藥貢獻了海西新藥超過九成的收入,達到4.25億元。
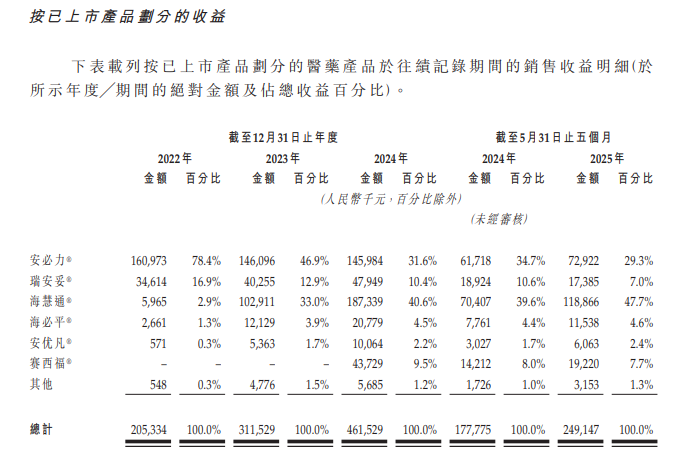
截圖自公司招股書
海西新藥提到,旗下各類產品在全國得以成功商業化,得益於專業高效的銷售團隊、全國性的銷售及分銷網絡以及多維度的銷售模式,觸達全國約1.8萬家醫院及其他醫療機構以及2.2萬家藥店。
值得一提的是,截至招股書披露日,海西新藥共有202名員工,其中研發、行政團隊分別為112人、54人,銷售團隊僅有36人,公司稱他們「平均擁有約十年製藥行業經驗」。
學霸夫妻執掌41.17%股份
募資8.6億元加碼創新藥
回顧海西新藥的孖展歷程,早在2022年11月,該公司就與海通證券簽署了輔導協議,向證監會提交了上市輔導備案申請,計劃衝刺A股上市。之後,海西新藥選擇轉戰港股,並於今年年初向港交所遞交招股書,但六個月後因申請自動失效,首次衝刺未果。8月6日,海西新藥再次向港交所遞交招股書。
招股書顯示,海西新藥共同創始人、董事長康心汕今年54歲,1993年獲得中國科學技術大學高分子化學學士學位,1999年獲得普林斯頓大學化學博士學位,在製藥行業擁有超過26年經驗,曾在貝達藥業(300558.SZ)擔任首席藥學家。其妻子Feng Yan(加拿大籍)先後畢業於蘭州大學、中國科學院,目前為公司執行董事、副總經理。
2012年3月,康心汕與Feng Yan聯合福建省三大國有資產平台(大同創業、福州投資及華僑實業)共同發起設立了海西新藥。2017年,海西新藥股權結構發生調整,三家國有股東將40%的股權以2000萬元的對價轉讓給康心汕。同年,康心汕出任公司董事長。
截至招股書披露日,康心汕與Feng Yan合計持有公司41.17%股份。
從海西新藥的發展戰略來看,該公司將繼續通過銷售仿製藥以支持創新藥研發。目前,該公司有4款在研創新藥產品管線,涵蓋腫瘤、眼科、呼吸疾病等適應症。此外還有5款仿製藥處於ANDA(仿製藥註冊申請)階段,預計將於2025年或2026年獲得上市批准。
據海西新藥披露的全球發售文件,公司最終發售定價為86.40港元/股,募資淨額9.4億港元(約合人民幣8.6億元)。海西新藥此前表示,募資將分別用於持續投資研發,推進公司管線中的在研藥物並豐富公司的產品組合,以及用於提升公司的研發能力及尋求合作機會、公司的營運資金及其他一般企業用途、增強公司的商業化能力及擴大市場影響力等。
從招股書來看,該公司4款在研創新藥均處於臨床早期階段。其中進度最快的C019199,是一款多靶點腫瘤免疫調節劑,適應症包括骨肉瘤、乳腺癌、結直腸癌、胰腺癌及TGCT(腱鞘鉅細胞瘤)等。從最快進度來看,骨肉瘤治療已完成I期臨床並啓動II期臨床試驗,預計於2025年下半年啓動III期臨床試驗。
紅星新聞記者蔣紫雯
(文章來源:紅星資本局)