智通財經APP獲悉,國家藥品監督管理局藥品審評中心公開信息顯示,東陽光藥(06887)自主研發的siRNA療法——HECN30227已獲臨床試驗默示許可,批准開展慢性乙型肝炎(以下簡稱乙肝)適應症的臨床試驗。目前全球尚無乙肝siRNA藥物獲批上市。
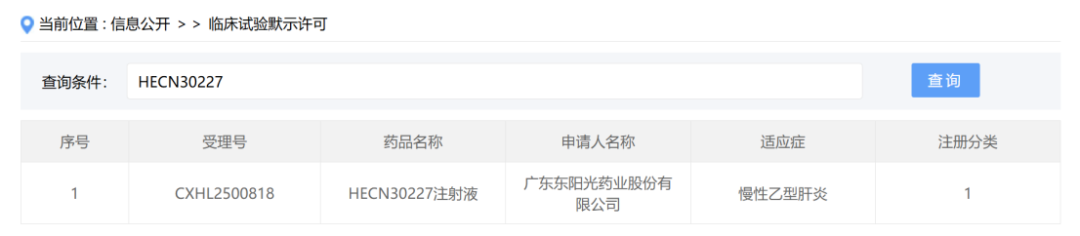
圖1:HECN30227獲批開展慢性乙肝適應症的臨床試驗
慢性乙肝是嚴重的全球公共衛生問題,我國患者基數龐大,約有7500萬例慢性乙肝病毒(HBV)感染者[1],疾病負擔沉重。現有的核苷(酸)類似物和干擾素治療方案雖能抑制HBV複製,改善肝組織病理學,但難以實現功能性治癒,且存在副作用大或需長期服藥等侷限。在這種情況下,亟需開發新型治療方案。
HECN30227是東陽光藥自主研發並擁有全球知識產權的1類新藥,也是公司基於小核酸技術平台開發的首款siRNA藥物,可同時消除cccDNA和intDNA來源的乙肝表面抗原(HBsAg)。臨床前數據表明,HECN30227具有泛基因型活性,可高效降低HBsAg水平,對核苷類藥物耐藥株同樣保持突出藥效,體內外藥效亦優於臨床競品。
該藥物採用東陽光藥獨特設計的HEC-GalNova(N-乙酰半乳糖胺)肝靶向遞送系統,在實現精準高效肝臟遞送的同時大幅降低脫靶風險。基於對HBV清除機制的深刻了解,公司正同步開發「siRNA+ASO+免疫調節劑」三聯療法,通過多靶點協同作用全面抑制HBV和HBsAg,並通過免疫重建開啓乙肝「功能性治癒」新時代,為患者帶來新希望。
近日,HECN30227與公司自研的高選擇性hTLR8免疫激動劑臨床前聯合用藥的重要研究成果,入選2025年美國肝臟疾病研究學會年會(AASLD)「Poster of Distinction」,該稱號僅授予評分位列前10%的成果,標誌着國際權威學術機構對HECN30227聯用組合臨床開發潛力的高度認可。

圖2:HECN30227與高選擇性hTLR8免疫激動劑臨床前聯合用藥研究成果入選AASLD 「Poster of Distinction」
東陽光藥持續聚焦抗感染領域,依託自主構建的小核酸技術與遞送平台,不斷推進以HECN30227為核心的功能性治癒策略。未來,公司將繼續深化「多靶點聯合」的研發路徑,積極探索該療法在更廣泛患者羣體中的臨床應用潛力,致力於為中國乃至全球的乙肝患者提供可及、可愈的創新治療方案。
參考文獻:
[1] 鄧優,孟彤彤,尤紅,等. 中國乙型肝炎最新流行病學及防治進展. 中華肝臟病雜誌,2025,33(02):115-120.