近日,華領醫藥研發的2型糖尿病創新藥——多格列艾汀獲香港衛生署藥物辦公室批准上市,成為香港「1+」新藥審批機制下獲批的首個普藥(適用人群廣泛的常見病藥品)。2023年,這家上海企業通過解放日報向有關部門反映了「國產創新藥在香港上市難」問題。如今,他們心願達成,這款創新藥已「直通」香港。憑藉內地和香港兩張藥品註冊證,公司計劃出海東南亞,為國產創新藥開闢廣闊的海外市場。
香港曾長期實行「2+」新藥審批機制,規定一款新藥須先在2個「清單國家」上市,才能在港申請註冊。這份清單裏,絕大多數是發達國家。在中國內地上市的創新藥要進入香港,不得不先到這些國家申請註冊,難度很大。
可否改革這一制度,推動在內地上市的國產創新藥更快進入香港?2023年8月,華領醫藥創始人、首席執行官陳力博士通過解放日報,表達了他的心聲。
他告訴記者,這一制度是歷史原因造成的。中國曾是「仿製藥大國」,在創新藥研發和註冊領域與一些發達國家有很大差距。然而過去十餘年,我國生物醫藥研發實力快速上升,國產創新藥持續問世。2017年,中國藥監部門加入ICH(人用藥品技術要求國際協調理事會),在註冊標準等方面已與發達國家接軌。
多格列艾汀就是國產創新藥的一個代表,它誕生於上海張江,是全球首創、中國首發的葡萄糖激酶激活劑類口服降糖藥,可從源頭上提升糖尿病患者的葡萄糖敏感性,改善血糖穩態失調。
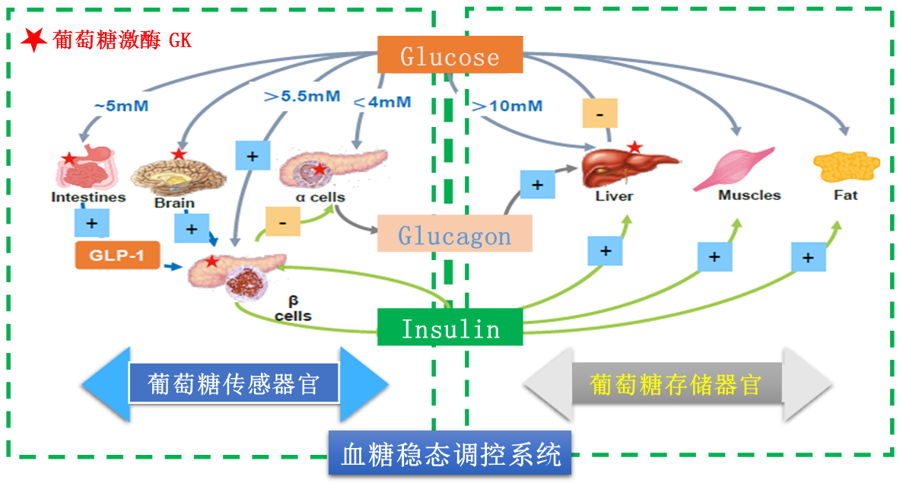
多格列艾汀治療2型糖尿病的科學原理
讓陳力欣喜的是,2023年11月,香港衛生署開始實施新的「1+」新藥審批機制,規定嚴重或罕見疾病新藥(特藥)只要在1個「清單國家」上市,即可申請註冊,中國國家藥監局也在清單中。雖然多格列艾汀屬於普藥,無法享受這項政策,但制度改革已經啓動。一年後,香港就將「1+」機制擴展到所有新藥。
2025年初,華領醫藥向香港衛生署提交了香港、內地醫學專家推薦材料。9月,香港衛生署正式受理多格列艾汀的新藥上市申請。經過政府與公司十餘輪問答,審評工作今年2月完成。本月,公司發布了多格列艾汀將惠及香港糖尿病患者的好消息。
未來,華領醫藥將以香港為出海樞紐,開拓總人口約7億的東南亞市場。「香港與新加坡、泰國、菲律賓等國家藥監部門聯繫緊密,獲得中國內地和香港的藥品註冊證後,我們能更便捷地進入這些國家的新藥註冊通道,在國際化佈局中邁出關鍵一步。」陳力說,這一國際化佈局對我國醫藥企業有參考價值:國產創新藥在中國內地上市後,可申請在香港上市,隨後憑「兩證」出海東南亞,為衆多國外患者帶來新的治療選擇。
(文章來源:上觀新聞)