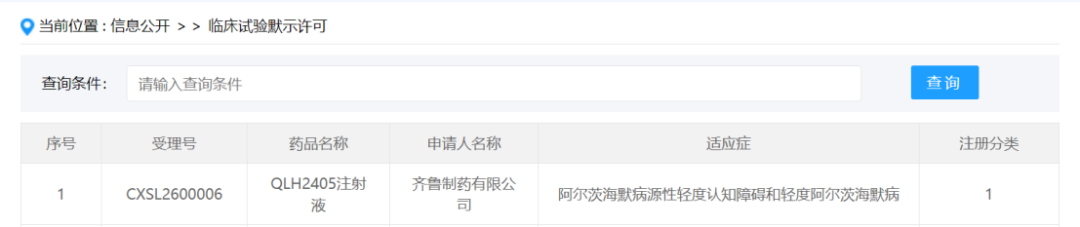
3月13日,據國家藥品監督管理局藥品審評中心(CDE)官網顯示,齊魯製藥自主研發的1類新藥QLH2405注射液獲得臨床試驗默示許可,擬定適應症為阿爾茨海默病源性輕度認知障礙和輕度阿爾茨海默病。
阿爾茨海默病是全球發病率最高的神經退行性疾病,相關統計數據表明,目前我國阿爾茨海默病患者已近千萬,佔全球的25%—30%。作為一種慢性、進行性神經退行性疾病,阿爾茨海默病起病隱匿且早期干預窗口極為關鍵。
齊魯製藥始終以患者為中心,致力於解決未被滿足的臨床需求。QLH2405注射液瞄準疾病發展早期的輕度認知障礙階段,旨在從源頭探索延緩疾病進展的新路徑。這款生物藥獲批臨床,標誌着齊魯製藥在中樞神經系統(CNS)疾病領域的研發管線進一步豐富,也是神經科學領域的又一個重要里程碑進展。

在申報過程中,齊魯製藥嚴格按照藥品審評相關法規要求,系統性地提交了藥學研究、藥理毒理評價及臨床擬用方案等全套申報資料。獲批臨床後,齊魯製藥將繼續秉持科學、嚴謹、規範的原則,加快推進臨床試驗,力爭全面評估QLH2405注射液在目標人群中的安全性及有效性。
面對我國日益嚴峻的人口老齡化趨勢,齊魯製藥將持續加大在阿爾茨海默病等重大疾病領域的技術攻關,堅持做有溫度的創新,不斷研發出更多高質量的臨床亟需藥物,惠及廣大患者及其家庭。