智通財經APP獲悉,據港交所3月25日披露,邁威(上海)生物科技股份有限公司(邁威生物(688062.SH))向港交所主板遞交上市申請書,中信證券和海通國際為聯席保薦人。這是該公司第二次遞表港交所。招股書顯示,截至最後實際可行日期,邁威生物已有三款商業化的生物類似藥產品,即邁利舒®、邁衛健®及君邁康®。
中介團隊
公司簡介
據招股書,邁威生物成立於2017年,是一家以藥物研發方面的創新能力以及從藥物發現至商業化銷售的端到端能力而聞名的中國製藥公司。該公司A股自2022年1月起在上海證券交易所科創板上市(股票代碼:688062)。公司的核心產品9MW2821(bulumtatug fuvedotin (「BFv」))是一款靶向Nectin細胞黏附分子4(「Nectin-4」)的抗體偶聯藥物(「ADC」)(「靶向Nectin-4 ADC」)。此外,該公司已建立包括13個以上不同品種的藥物資產的管線產品組合。
邁威生物的自研核心產品9MW2821是一款ADC技術產品。根據弗若斯特沙利文的資料,截至最後實際可行日期,就臨床開發階段而言,9MW2821是在中國開發的用於治療尿路上皮癌(「尿路上皮癌」)的所有靶向 Nectin-4 ADC中進展最快的,在全球僅次於Padcev(唯一經FDA批准的靶向Nectin-4 ADC)。根據同一數據源,9MW2821也是全球首款進入宮頸癌(「宮頸癌」)關鍵III期試驗階段的靶向Nectin-4 ADC。該公司正在進行9MW2821的多項臨床試驗,其中包括(i) 9MW2821分別作為單藥療法及聯合特瑞普利單抗(一款獲批用於治療包括多種實體瘤在內的適應症的PD-1抗體藥物)治療尿路上皮癌的III期試驗;(ii) 9MW2821作為單藥療法治療宮頸癌的III期試驗;(iii) 9MW2821作為單藥療法或聯合特瑞普利單抗治療三陰性乳腺癌(「三陰性乳腺癌」)的II期試驗;及(iv) 9MW2821單藥治療晚期食管癌的II 期臨床試驗。截至最後實際可行日期,邁威生物已在全球範圍內獲得140項專利並提交276 份專利申請,包括與核心產品有關的25項專利及17份專利申請。
邁威生物持續開發及升級ADC藥物開發平台、一體化高效抗體發現平台及TCE雙╱三特異性抗體開發平台等技術平台。上述技術平台的建立,旨在支持新候選藥物的發現和開發。 2025年5月,邁威生物的首款商業化創新藥邁粒生® (研發代號:8MW0511)獲國家藥監局上市批准。邁粒生®獲批用於成年非髓性惡性腫瘤患者在接受容易引起發熱性中性粒細胞減少症的骨髓抑制性抗癌藥物治療時,降低以發熱性中性粒細胞減少症為表現的感染發生率。
同時,鑑於生物類似藥的研發周期通常明顯短於創新生物藥,且能在相對較短時間內為公司創造收入,邁威生物積極把握生物類似藥的開發和商業化機會。截至最後實際可行日期,邁威生物已有三款商業化的生物類似藥產品,即邁利舒®、邁衛健®及君邁康®。 2025年8月,邁利舒®及邁衛健®獲巴基斯坦藥品監管局上市批准。邁利舒®及邁衛健®是在巴基斯坦獲批的首個Prolia®及Xgeva®生物類似藥。2025年12月,君邁康®在印度尼西亞獲批上市。
截至最後實際可行日期,邁威生物並無任何已商業化產品獲選納入中國國家藥品集中採購計劃下的藥品採購目錄。此外,該公司已商業化產品的同類產品亦無獲選納入集中採購計劃下的藥品採購目錄。中國的藥品集中採購計劃(國家層面)主要側重於化學藥品及中藥,而公司的現有已商業化產品並不涵蓋該等類別。
邁威生物已建立擁有自主知識產權的四大核心ADC技術:DARfinity,邁威生物自主研發的定點偶聯工藝;IDconnect,一種經過優化設計的連接符分子,用以連接抗體和毒素,使抗體和毒素之間的連接更穩定;Mtoxin,一類基於喜樹鹼的新型毒性分子,用作ADC中殺死靶細胞的「彈頭」;及LysOnly,一種能夠有條件釋放毒素的結構,可提高ADC的整體安全性和有效性。此外,邁威生物已開發其他技術平台:一體化高效抗體發現平台和TCE雙╱三特異性抗體開發平台。
財務資料
收入
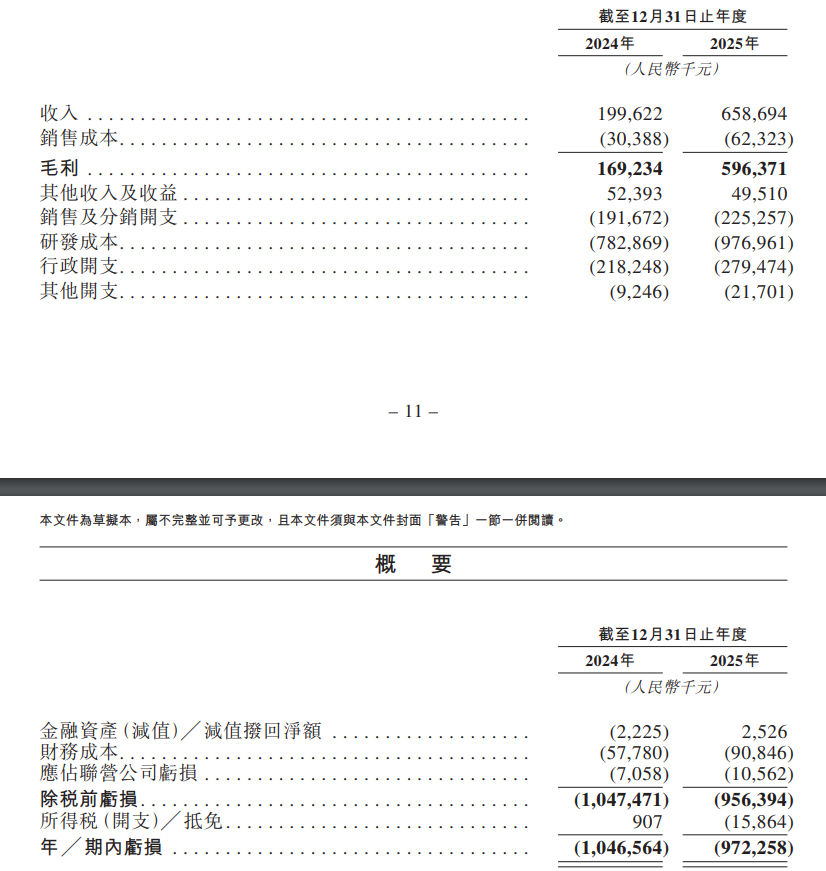
於2024年度、2025年度,公司實現收入分別約為2億元、6.59億元人民幣。
年╱期內虧損
於2024年度、2025年度,公司年╱期內虧損分別約為10.47億元、9.72億元人民幣。
行業概覽
腫瘤藥物的市場規模方面,2024年全球新增癌症病例2130萬例,預計截至2032年將達到2550萬例。截至 2024年,肺癌、乳腺癌和結直腸癌是全球發病率排名前三的癌症。在中國,截至2024 年,肺癌、結直腸癌和甲狀腺癌是發病率排名前三的癌症。全球腫瘤藥物市場規模從 2019年的1,435億美元增長到2024年的2,533億美元,複合年增長率為12.0%,預計將進一步增至2028年的3,759億美元及2032年的5,482億美元,2024年至2028年及2028年至 2032年的複合年增長率分別為10.4%及9.9%。中國腫瘤藥物市場也從2019年的264億美元增長到2024年的359億美元,複合年增長率為6.3%,預計將進一步快速增長到2028 年的543億美元及2032年的992億美元,2024年至2028年及2028年至2032年的複合年增長率分別為10.9%及16.3%。
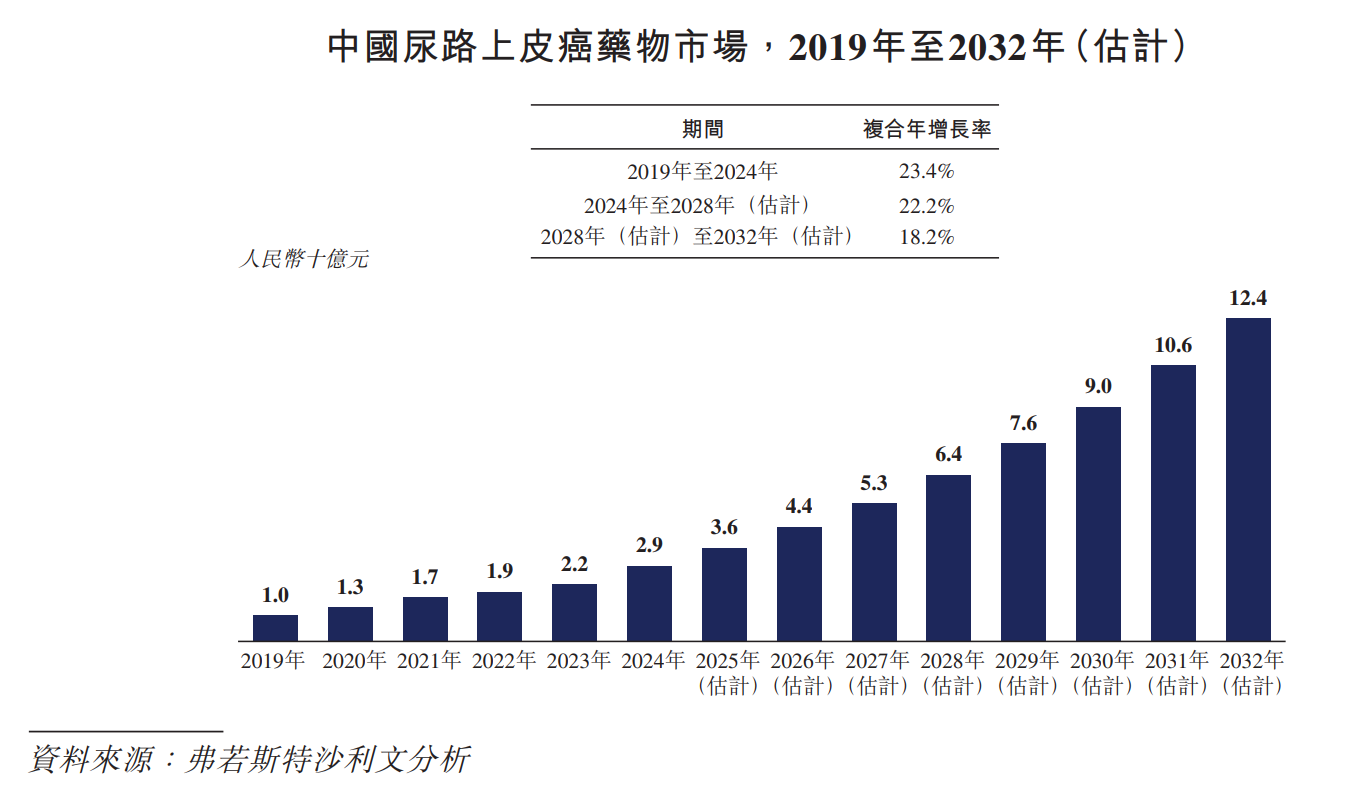
尿路上皮癌(「尿路上皮癌」)為截止目前最常見類型的膀胱癌,佔所有膀胱癌約 90%。該等癌症始於膀胱、輸尿管及腎盞內部的尿路上皮細胞。尿路上皮癌的全球發病率從2019年的508,200例增加至2024年的572,900例,預計將進一步增加至2028年的 634,200例及2032年的701,000例,2024年至2028年及2028年至2032年的複合年增長率分別為2.6%及2.5%。在中國,尿路上皮癌的發病率從2019年的76,300例增加至2024年的89,000例,預計將進一步增加至2028年的98,800例及2032年的108,600例,2024年至 2028年及2028年至2032年的複合年增長率分別為2.7%及2.4%。
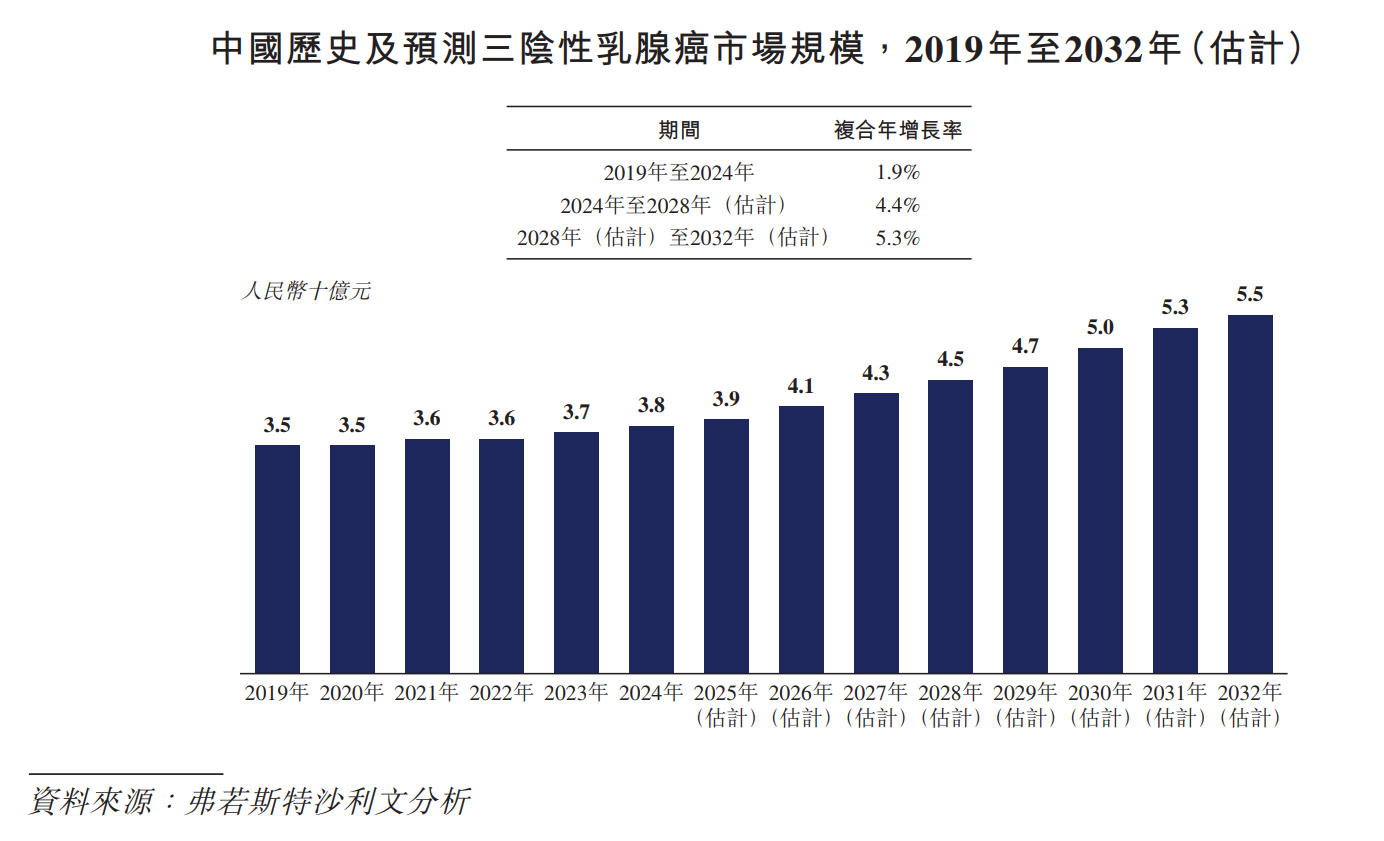
三陰性乳腺癌(「三陰性乳腺癌」)是指雌激素受體(「ER」)、孕激素受體(「PR」)及人類表皮生長因子受體2(「HER2」)均為陰性的一種乳癌。三陰性乳腺癌約佔全球所有乳癌病例的15%至20%,由於缺乏特定的治療靶點,通常被認為是惡性程度最高的一種亞型。三陰性乳腺癌通常更多在較年輕及絕經前的婦女中被診斷出來。三陰性乳腺癌的全球發病率從2019年的320,100例增加至2024年的364,900例,預計將進一步增加至2028年的382,400例及2032年的405,900例,複合年增長率分別為1.2%及1.5%。在中國,三陰性乳腺癌的患病人數從2019年的49,500例增加至2024年的55,900例,預計將進一步增加至2028年的58,600例及2032年的60,400例,2024年至2028年及2028年至 2032年的複合年增長率分別為1.2%及0.7%。
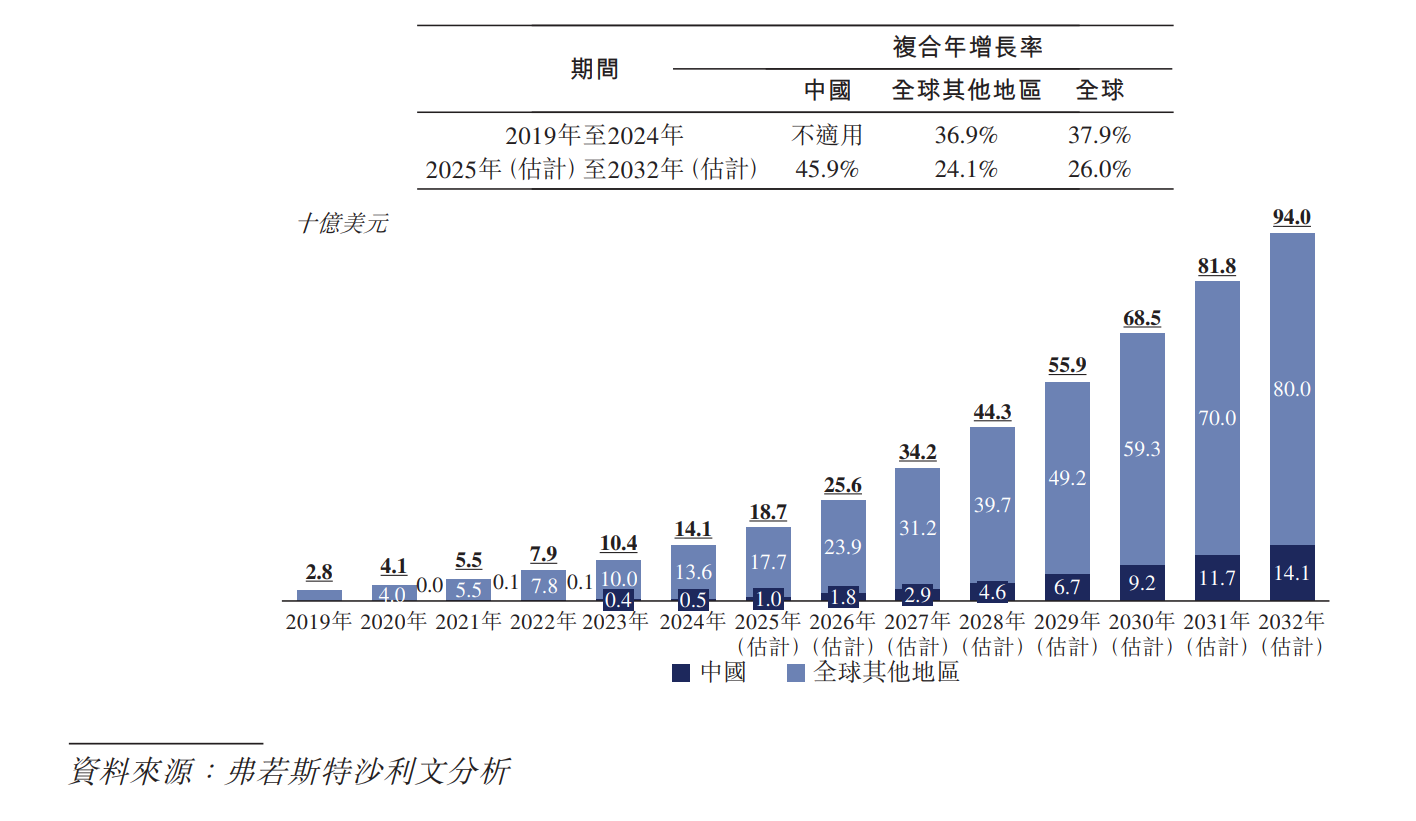
在全球範圍,2024年前五大商業化ADC藥物的年度銷售額均超過10億美元。
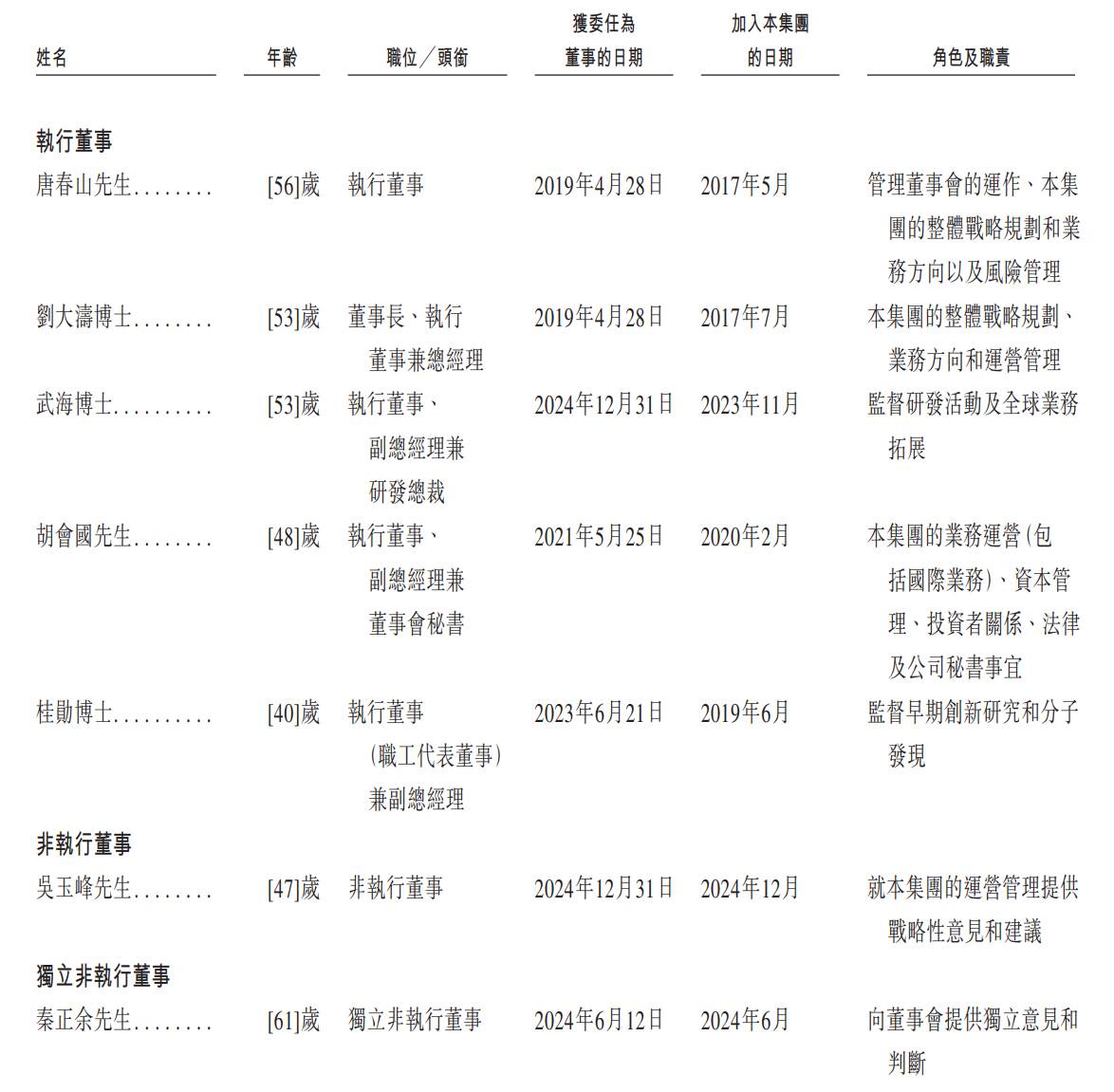
董事會資料
董事會由十名董事組成,包括五名執行董事、一名非執行董事和四名獨立非執行董事。董事任期三年,可連選連任。根據中國相關法律法規,獨立非執行董事連續任職不得超過六年。
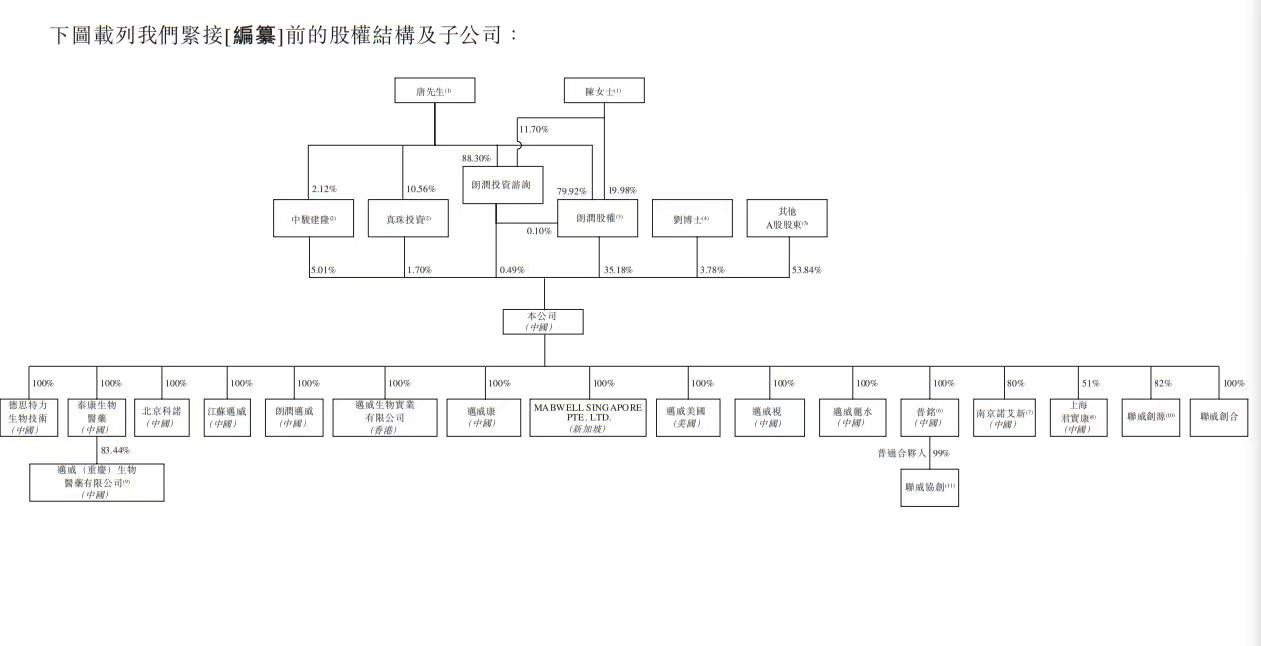
股權架構
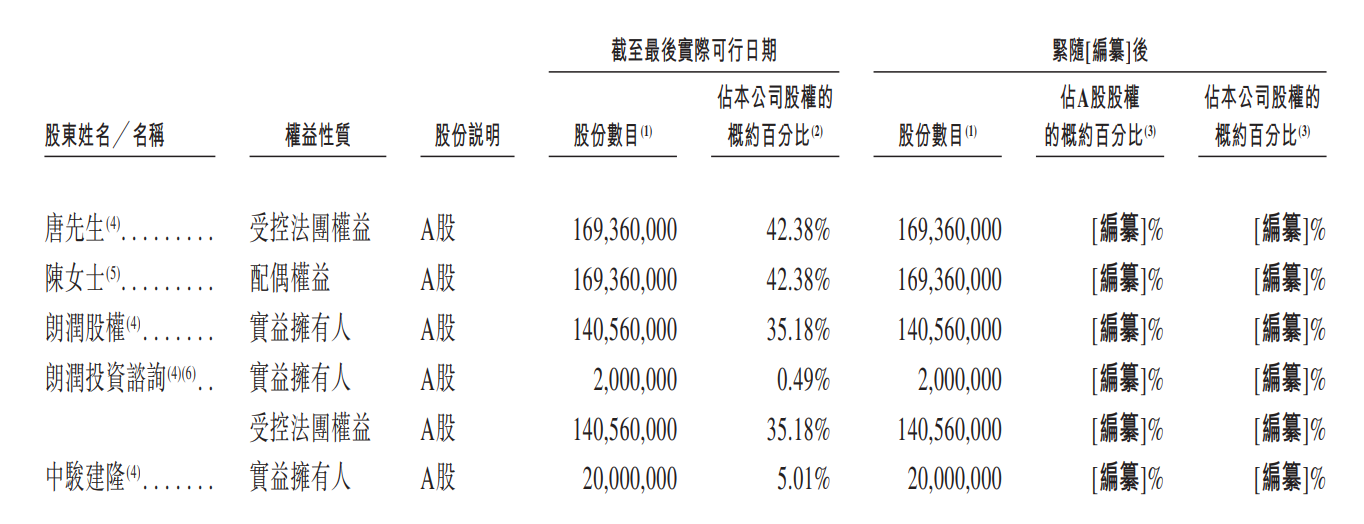
緊接[編纂]前,公司由(i)朗潤股權擁有約35.18%;(ii)中駿建隆擁有約5.01%; (iii)真珠投資擁有約1.70%;及(iv)朗潤投資諮詢擁有約0.49%。
朗潤股權為有限合夥企業,由執行董事唐春山先生、唐先生的配偶陳姍娜女士(彼等均為有限合夥人)及朗潤投資諮詢(亦為其唯一普通合夥人)分別擁有約79.92%、19.98%及 0.10%。朗潤投資諮詢分別由唐先生及陳女士擁有88.30%及11.70%。中駿建隆及真珠投資各自為員工激勵平台及有限合夥企業,由唐先生憑藉彼作為其各自唯一普通合夥人的地位而控制。據董事所深知,概無控股股東訂立任何與公司有關的一致行動或附屬協議。
因此,唐先生及陳女士透過控股股東朗潤股權、中駿建隆、真珠投資及朗潤投資諮詢合共控制公司已發行股本總額約42.38%,並於緊接[編纂]前就上市規則而言構成一組控股股東。
中駿建隆及真珠投資均為員工激勵平台及唐先生通過擔任其各自唯一普通合夥人控制的有限合夥企業。
朗潤股權為一家有限合夥企業,由唐先生及陳女士(作為有限合夥人)及朗潤投資諮詢(作為唯一普通合夥人)擁有。
中介團隊
聯席保薦人:中信證券(香港)有限公司、海通國際資本有限公司
公司法律顧問:Davis Polk & Wardwell、競天公誠律師事務所、霍金路偉律師行
聯席保薦人的法律顧問:史密夫斐爾律師事務所、金杜律師事務所
核數師兼申報會計師:安永會計師事務所
行業顧問:弗若斯特沙利文(北京)諮詢有限公司上海分公司
合規顧問:新百利孖展有限公司