专注于开发和商业化中枢神经系统(CNS)疾病新型疗法的生物制药公司 Axsome Therapeutics, Inc. 周三宣布,美国食品药品监督管理局(FDA)已对其提交的、旨在扩大其抑郁症疗法AXS-05(商品名:Auvelity)适应症至阿尔茨海默病激越症状的上市申请授予优先审评资格。该公司在一份声明中表示,针对AXS-05的补充新药申请,FDA已将2026年4月30日设定为目标审评完成日期。
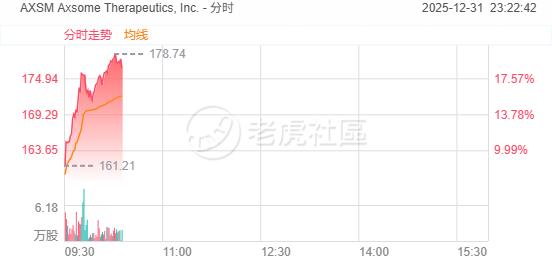
Axsome Therapeutics盘初拉升大涨超19%。
2022年,FDA批准AXS-05用于治疗成人重度抑郁症。2020年,FDA授予该药物治疗阿尔茨海默病激越症状的突破性疗法资格。资料显示,阿尔茨海默病(AD),又称老年性痴呆,是一种常见的神经系统退行性疾病。其发病机制复杂,主要表现为记忆力下降、认知功能减退、行为异常等。据报道,超过一半以上的AD患者存在激越症状,其特征是情绪困扰、言语和身体攻击性、破坏性易怒和脱抑制。激越是阿尔茨海默病(AD)患者的一种神经精神症状,这种情况通常在AD病程早期就开始出现并持续存在,这会增加医疗保健的费用,并显著增加护理人员的负担和患者的痛苦。
AXS-05(右美沙芬-安非他酮)是一种口服N-甲基-D-天冬氨酸受体拮抗剂、sigma-1激动剂和氨基酮CYP2D6抑制剂。AXS-05利用右美沙芬和安非他酮的专利配方和剂量,以及Axsome的代谢抑制技术,来调节成分的输送。AXS-05的右美沙芬成分是非竞争性NMDA受体拮抗剂,也称为谷氨酸受体调节剂和σ-1受体激动剂。AXS-05的安非他酮成分用于增加右美沙芬的生物利用度,并且是去甲肾上腺素和多巴胺再摄取抑制剂。这种新型疗法有望改善以情绪困扰、言语和身体攻击、破坏性易怒和脱抑制为特征的AD激越。
Axsome首席执行官Herriot Tabuteau表示:“我们非常高兴FDA受理并授予了我们的补充新药申请优先审评资格,该申请旨在将AXS-05用于治疗阿尔茨海默病激越症状。我们期待在接下来的审评阶段继续与FDA保持合作。”