2020年11月16日,康方生物-B(9926.HK)获得由格隆汇颁发的2020年最具创新力IPO奖。在今年4月成功登陆港交所之后的康方生物,在不到1个月时间在研产品派安普利单抗递交新药上市申请,8月成功纳入恒生综合指数、恒生医疗保健指数以及恒生香港上市生物科技指数等成分股。上市至今,Cadonilimab双抗等核心产品临床进度高效推进,商业化进程迅速铺开。
康方生物上市已有半年之余,借此次获得最具创新力IPO,我们来梳理一下,这家生物医药公司的创新力在哪里?
图表一:公司获2020年度最具创新力IPO奖
图片来源:格隆汇
双抗赛道领头羊,研发迅速推进
根据公开披露数据,依托科学家团队强大的研发实力,康方生物建立了超过20个用于治疗肿瘤、自身免疫、炎症、代谢疾病等重大疾病的创新药物产品管线,包括两个国际首创的双特异性抗体新药(PD-1/CTLA-4以及PD-1/VEGF)。其中10个品种开启了超过40项临床研究项目。管线涵盖了PD-1、CTLA-4、VEGF、CD47、CD73、IL-12/IL-23、IL-17、IL-4R等创新靶点。
Cadonilimab(PD-1/CTLA-4,AK104):有望成为全球首个获批的基于PD-1的双抗药物
PD-(L)1和CTLA-4都是目前全球热度最高的免疫治疗靶点,据公开数据,PD-1和CTLA-4联合治疗对某些难以治疗的癌症类型产生了显著改善的总体缓解率(ORR),包括肾细胞癌、胃癌、小细胞癌肺癌等。但是这种联合疗法存在较为明显的毒副作用,由此也限制了联合疗法更加广泛的应用。正因联合用药的疗效和毒副作用,科学家希望通过双抗的设计,在保留或者提升联合用药疗效的同时,显著提升药物的安全性。目前全球范围内基于PD-(L)1的双抗已有众多跨国公司巨头正在布局,但尚无产品获批上市。
康方生物的Cadonilimab(PD-1/CTLA-4,AK104)是目前研发进展最快的产品,2020年3月Cadonilimab单药治疗宫颈癌及5月Cadonilimab单药治疗鼻咽癌分别在美国和中国启动关键注册性II期临床。
2020年10月,康方生物全球首创的新型肿瘤免疫治疗双特异性抗体新药Cadonilimab(PD-1/CTLA-4,AK104)用于治疗复发或转移性宫颈鳞癌,获得国家药品监督管理局(「NMPA」)药品审评中心(CDE)审核同意,纳入“突破性治疗品种公示”名单。而在此前2020年6月,Cadonilimab就已经被美国FDA授予了快速审批通道资格。
如果进展顺利,Cadonilimab将有望成为全球获批上市的首个基于PD-1的双特异性抗体药物。
而Cadonilimab之所以能够在同时快速地获得美国和中国药品监管部门高度认可,则是基于Cadonilimab优异的临床数据。根据康方生物发布的Cadonilimab用于二线/三线治疗宫颈癌临床最新数据显示,AK104治疗晚期宫颈癌的ORR(客观缓释率)高达为47.5%,远高于现有PD-1/CTLA-4单药或联合用药数据,在疗效上有显著的提升。安全性与联合用药相比也有明显提升,与已经公布数据的PD-1相当。
美国调研机构预测CTLA-4与PD-1联合用药的潜在市场规模权威机构预测年销售规模峰值有望达到133亿美元。Cadonilimab的最新数据则预示着该药未来的市场空间将很有希望超越联合用药。
图表二:AK104用于治疗晚期宫颈癌临床II期数据
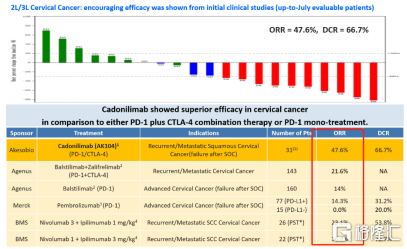
数据来源:公开资料,格隆汇整理
目前,Cadonilimab正在澳大利亚、新西兰、美国开展二线/三线治疗复发或转移性宫颈癌的单臂注册性临床试验。主要适应症还包括肝癌、胃癌、肺癌、食管鳞癌及鼻咽癌等。
AK112(PD-1/VEGF双抗):对PD-1不敏感型实体瘤患者效果良好
AK112是康方生物自主研发另一款全球首个进入临床研究的PD-1/VEGF双特异性抗体。
从药物设计上来看,AK112是基于康方生物独特的TETRABODY技术设计,可阻断PD-1与PD-L1和PD-L2的结合,并同时阻断VEGF与VEGF受体的结合。鉴于VEGF和PD-1在肿瘤微环境中的共表达,与联合疗法相比,AK112作为单一药物同时阻断这两个靶点,可能会更有效地阻断这两个通路从而增强抗肿瘤活性。
目前AK112已经在澳洲和中国开展Ia期临床研究。AK112的Ia期研究阶段性数据10月已在2020中国肿瘤免疫治疗会议上发布。
研究的结果显示,在有至少经历过一次肿瘤评估并对PD-1抑制剂不敏感或接受过PD-1抑制剂治疗的11例晚期实体瘤患者中,共有4例达到了缓解(客观缓解率(ORR):36%),共7例肿瘤缩小且疾病稳定(疾病控制率(DCR):64%)。
特别值得注意的是,上述数据表明PD-1/VEGF双抗(AK112)有潜力成为突破性的疗法,为PD-1抑制剂不敏感或接受过PD-1抑制剂治疗的病人带来新的希望。
另外,与联合治疗相比,AK112能更特异性的在肿瘤组织局部富集,靶向阻断肿瘤局部的VEGF,解除免疫抑制的微环境,创造一个有利于PD-1发挥作用的微环境,协同抑制PD-1的功能,解除肿瘤细胞对T细胞免疫反应的抑制,发挥最大的抗肿瘤作用,这一理论假设在本临床研究中得到了初步验证。在联合免疫治疗时代,AK112治疗前景非常值得期待
图表三:AK112产品研发进程
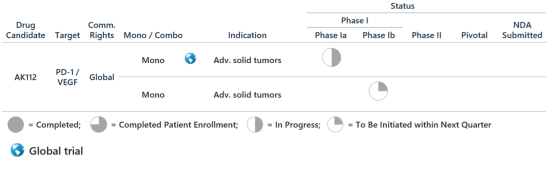
数据来源:公司资料,格隆汇整理
AK117(CD47抗体):第二代CD47产品T-cell占位效果最优,无贫血症状
CD47靶点是近期比较热门靶点,今年一季度吉利德以约49亿美元的天价收购拥有Hu5F9-G4(CD47单抗,第一代CD47代表产品)的Forty Seven公司,掀起业界对CD47追捧的热潮。
康方生物在近日召开的SITC会议上首次披露了其自主研发的第二代CD47单抗(AK117)的人体临床研究进展。
研究显示,所有正在进行的剂量爬坡队列中未发生药物相关的贫血症状,因此与第一代产品相比,无需使用低剂量诱导。且各队列受试者对药物耐受性良好,无剂量限制性毒性(DLT)事件发生。更重要的是,在药物活性指标方面,受试者外周血T细胞的CD47的受体占有率(RO)在3mg/kg队列就已经达到并维持在100%。
初步数据预示着,作为第二代CD47产品,康方生物AK117通过研发设计可能有潜力能够解决CD47最常见的严重血液不良反应问题,从而获得更好的安全性。低剂量即体现了极高的药物活性,预示着其疗效方面也具备潜力优势。AK117很有潜力成为CD47赛道下一颗闪亮的星。
目前,AK117的20mg/kg QW剂量组正在筹备中。
图表四:国内上市CD47抗体爬坡数据对比
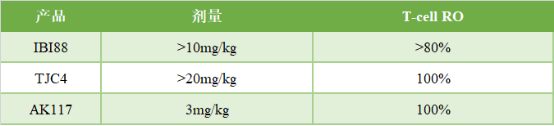
数据来源:公开资料,格隆汇整理
AK119(CD73抗体):新西兰用于治疗COVID-19的临床试验完成首例健康受试者给药
AK119是人源化单克隆抗体药物,可有效地引起B细胞活化并加强抗体产生,抑制CD73的酶学活性。
根据临床前数据显示,AK119可通过不同于抑制CD73酶活性的途径,上调B细胞活化的两个早期标记分子(CD69和CD83)的表达,还可促进B细胞产生免疫球蛋白M(IgM)和免疫球蛋白G(IgG)抗体。COVID-19患者增加抗体产生或可会加强彼等消除SARS-CoV-2病毒的能力。因此,AK119或会是治疗COVID-19疾病的有效方法。此外,AK119亦可能使人体对SARS-CoV-2病毒产生更强的免疫力,并可能与健康人士接种的疫苗结合使用,以增强疫苗的效力。
目前,AK119在美国用于治疗轻中度COVID-19患者的临床试验已经获得美国FDA的反馈,同意公司递交新药临床试验申请。今年10月,AK119在新西兰的临床试验完成COVID-19首例健康受试者给药。
另外,AK119还将与Cadonilimab联用,探索治疗实体瘤、胰腺导管腺癌、结直肠癌等重大疾病。
派安普利(PD-1单抗):潜在Best-in-Class单克隆抗体,中国新药上市申请阶段
派安普利单抗是由康方生物与中国生物制药旗下正大天晴共同开发和商业化的重组人源化抗PD-1单克隆抗体。相较于市面上已经销售的PD-1抗体,派安普利具有结构设计独特,临床试验数据优秀。
从研发进展上来看,今年5月,派安普利在用于治疗复发/难治疗性经典霍奇金淋巴瘤(r/r cHL)已经向国家药监局递交新药上市申请,预计2021年获批上市。今年10月,派安普利用于治疗三线鼻咽癌到达了主要临床重点,并获得美国食品药品监督管理局(FDA)授予的快速审批通道资格(FTD)。
临床研究数据方面,派安普利单抗至少进行了2次疗效评估的r/r cHL受试者中表现出了显著的临床获益。其中,客观缓解率(ORR)达到83.6%。完全缓解率(CR)达到49.3%,明显高于历史对照,也优于有条件上市的PD-1单抗;在治疗转移性鼻咽癌方面,经确认的ORR为27.0%,疾病控制率(DCR)为49.5%。安全性方面也优于市售PD-1单抗产品或相当。
此外,派安普利更多大适应症的拓展也已经进入到中后期阶段。其中派安普利和化疗联用治疗一线鳞状非小细胞肺癌完成了临床III期入组,一线非鳞非小细胞肺癌联用化疗和联用安罗替尼处于临床III期,非小细胞肺癌的新辅助/辅助疗法+化疗/+安罗替尼也处于临床II期,和化疗、安罗替尼联用治疗肝癌、胃癌等大适应症的临床在同时进行。
优异的临床疗效+大适应症后期临床快速推进+中国生物制药强大的专业销售能力,派安普利有望成为国内PD-1领域的主角。
图表五:AK105产品研发进程
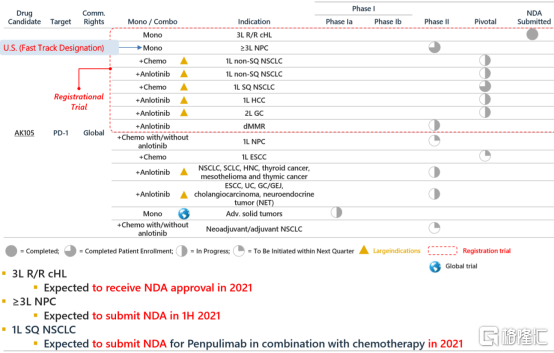
数据来源:公开资料,格隆汇整理
小结
整体来看,相较于刚上市时候的康方生物,如今的康方在产品管线上做了多项更新。无论是新药上市申请的递交,还是临床研发进度,一切都在向商业化进程上不断推进。
之所以可以称得上具有创新力,一方面的原因来自于其在双抗赛道深远布局和高效推进,另一方面原因来自于其研发项目均为自主研发项目,所有主推产品全部顺利进入临床只中后期,且与同靶点药物相比体现出更好的疗效或安全性。
肿瘤免疫疗法因疗效好、副作用小、复发率低的优点,被称为肿瘤治疗的第三次革命。基于PD-1的双抗产品,则是被学术界共同认可的肿瘤免疫疗法未来最具潜力的领域。于康方而言,最快的双抗产品Cadonilimab已经进入新药上市申请阶段,倘若成功获批,Cadonilimab将成为全球首个以PD-1作为基础的双抗药物,企业价值空间将会被进一步打开。更多如CD47、CD73等潜力巨大靶点的迅速推进和优势数据结果,更加突出了康方生物在抗体药物领域的创新实力和商业化潜力。
对于研发能力,尤其是一家创新药企,通常而言有两条路可以选,一种是自我研发,利用公司内部的研发实力,从而获得具有竞争力的创新药,另一种则是通过外部引进的方式,来完善公司的研发管线。康方生物是一家实打实通过自我研发走出国门的药企,成为了中国第一家向全球制药巨头默沙东授权自主研发抗体许可的中国生物科技公司。而这样的研发实力,或许在未来还将带来不一样的惊喜。
从上市以来的公司股价表现来看,公司股价在上市受到投资者的关注与追捧,截止发稿日,上市以来最高股价达到38.95港元/股,区间涨幅最高达到140.74%。
基于康方生物在生物制药领域的强大研发实力和高效进度,各大券商对于公司未来的发展仍然非常看好。其中,摩根大通与摩根士丹利均给予“增持”评级,中金公司给予“跑赢行业”评级,交银国际以及大和给予“买入”评级,最高目标价达到45港元/股,高于此前公司最高股价,值得持续关注与期待。
图表六:券商评级
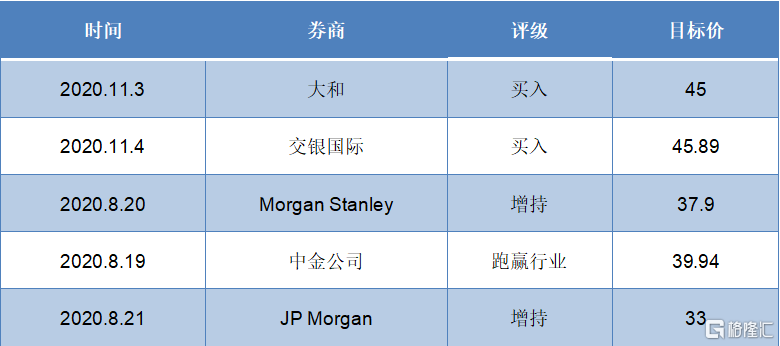
数据来源:WIND,格隆汇整理