金吾财讯 | 根据中国疾控中心的数据,2022年至2023年流感季中国的整体流感疫苗接种率为3.8%,与美国等发达市场相比较低。简而言之,中国流感疫苗市场巨大,但当前渗透率极低。
在此背景下,中慧元通生物科技股份有限公司致力于创新疫苗及采用新技术方法的传统疫苗的研发、制造及商业化。公司凭借四价流感病毒亚单位疫苗(商品名:慧尔康欣)作为核心产品,籍以申请上市加强产品的开发及国内外注册。
招股书显示,2023年6月公司向中国证监会提交了A股上市申请,但未被中国证监会正式受理。后于同年9月主动撤回向科创板作出的申请。公司于今年1月24日申请于港交所上市。而中国证监会确认公司已于今年6月25日完成备案。
公司创始人、董事长安有才拥有超35年管理经验,其中生物科技及制药行业经验逾15年。有趣的是,安有才早年最先涉足建筑工程领域,1987年7月毕业于中国唐山工程技术学院(现称华北理工大学),主修工业工程,于2010年起开始涉足生物科技行业,在多家生物科技公司担任管理职务,2015年创立中慧元通,负责战略规划与日常运营。
公司名称:江苏中慧元通生物科技股份有限公司
保荐人:中信证券、招银国际
控股股东:安有才、江苏粜宇、何一鸣
截至最后实际可行日期,由安有才、江苏粜宇及何一鸣组成的一致行动人士集团共同拥有约35.84%的股份权益,根据一致行动人士协议,于股东会或董事会会议上一致表决前,何一鸣须与安有才及江苏粜宇达成一致意见,如各方未能达成一致,何一鸣须遵循安有才及江苏粜宇的指示;江苏粜宇凭藉其作为各员工持股平台的普通合伙人的角色,被视为于员工持股平台持有的股份中拥有约9.72%权益。因此,一致行动人士集团及员工持股平台构成公司的控股股东集团,截至最后实际可行日期合共持有约45.55%的股份。
基本面情况:
公司是一家总部位于中国的疫苗公司,致力于创新疫苗及采用新技术方法的传统疫苗的研发、制造及商业化。截至最后实际可行日期,公司有(i)两种核心产品,即四价流感病毒亚单位疫苗(其于2023年5月获中国国家药品监督管理局(国家药监局)批准用于三岁及以上人群,商品名慧尔康欣)及在研冻干人用狂犬病疫苗(其使用人二倍体细胞开发,具有良好的安全性);及(ii)其他11种在研疫苗,涵盖对疫苗接种有庞大需求的多个疾病领域。
公司的核心产品为四价流感病毒亚单位疫苗。其旨在针对两种甲型流感病毒(H1N1和H3N2亚型)和两种乙型流感病毒(Yamagata和Victoria谱系)提供广泛的保护。与全病原体疫苗或裂解疫苗相比,流感病毒亚单位疫苗仅含有病毒的关键成分,需要在病毒裂解后进一步纯化,从而有利于精准地靶向抗原,确保安全性更好、不良反应风险更低。因此,与全病原体疫苗及裂解疫苗相比,流感病毒亚单位疫苗(包括公司的四价流感病毒亚单位疫苗)的定价通常较高。
商品名为慧尔康欣的四价流感病毒亚单位疫苗于2023年5月获国家药监局的NDA批准,可用于三岁及以上人群。其成为截至最后实际可行日期在中国获批的首款且唯一一款四价流感病毒亚单位疫苗。
其他在研产品包括,三价流感病毒亚单位疫苗、23价肺炎球菌多糖疫苗(PPSV23)、重组带状疱疹疫苗(CHO细胞)及24价肺炎球菌结合疫苗(PCV24),用于预防肺炎球菌疾病;(ii)mRNA疫苗及重组疫苗,旨在预防呼吸道合胞病毒(RSV)感染;(iii)mRNA猴痘疫苗;(iv)水痘减毒活疫苗;及(v)吸附破伤风类毒素疫苗。
行业现状:
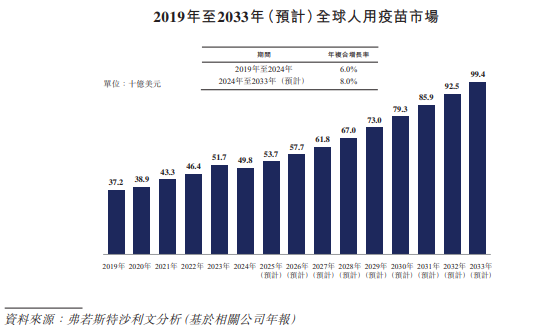
销售收入方面,不计入新冠肺炎疫苗的情况下,全球人用疫苗市场由2019年的372亿美元增加至2024年的498亿美元,年复合增长率为6.0%。在中国等新兴国家创新疫苗持续商业化及市场增长的驱动下,预计2033年全球人用疫苗市场将达到994亿美元,2024年至2033年的年复合增长率为8.0%。
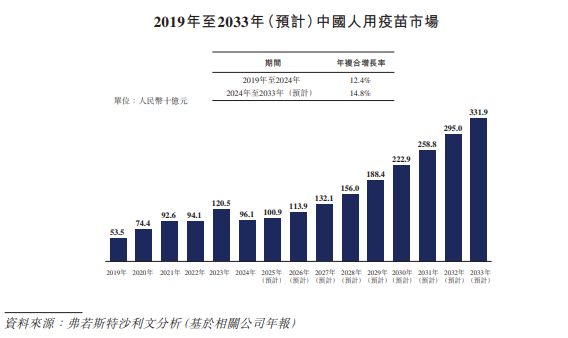
在产值方面,不计入新冠肺炎疫苗的情况下,中国人用疫苗市场由2019年的人民币535亿元增长至2024年的人民币961亿元,年复合增长率为12.4%。在创新疫苗预期持续推出的推动下,中国人用疫苗市场预期于2033年进一步增长至人民币3,319亿元,2024年至2033年的年复合增长率为14.8%。
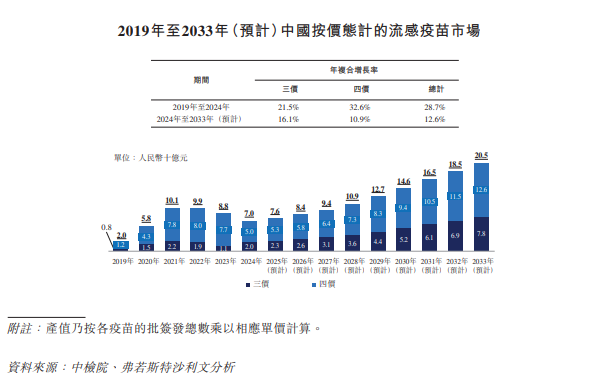
首个四价流感疫苗于2018年获国家药监局批准。自此,中国四价流感疫苗市场显著增长。批签发总数由2019年的9.7百万剂增加至2024年的46.6百万剂,年复合增长率为36.8%。由于新冠预防工作,2020年至2021年,流感市场规模短暂激增,导致生产商迅速扩大业务,增加批签发频率和数量。但2022年后,随着新冠疫情影响减弱,市场进入周期性调整阶段,批签发频率和数量略微减少,从而导致市场规模缩小。此外,于2024年,三价和四价灭活流感疫苗价格同时下降。因此,于2022年至2024年,中国流感疫苗的市场规模有所下降。
截至最后实际可行日期,中国有26种已上市的流感疫苗,主要包括13种三价疫苗(包括11种裂解疫苗、1种亚单位疫苗及1种减毒活疫苗)及12种四价疫苗(包括11种裂解疫苗及1种亚单位疫苗,即本公司的四价流感病毒亚单位疫苗)。
财务状况:
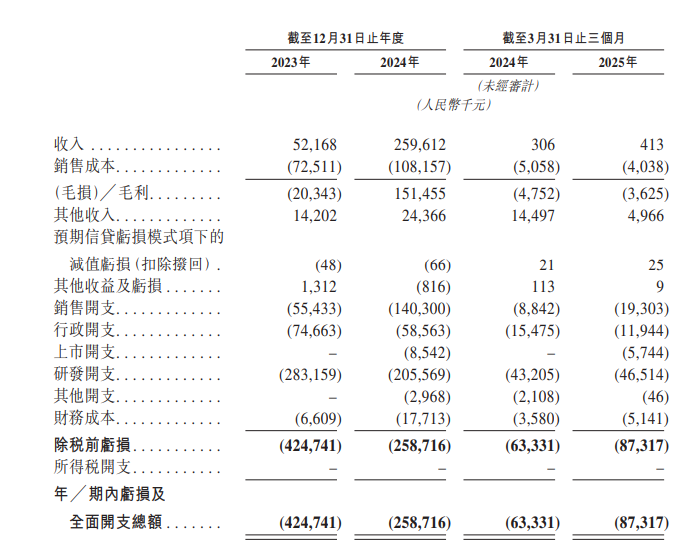
2023-2024财年,及2025年截至3月31日止三个月,公司分别录得收入5216.8万元(人民币,下同)、2.6亿元、41.3万元;对应同期,年内/期内亏损及全面开支总额分别为4.25亿元、2.59亿元、8731.7万元。
对应同期,研发开支为2.83亿元、2.06亿元、4651.4万元。其中,核心产品四价流感病毒亚单位疫苗及在研冻干人用狂犬病疫苗应占研发开支(i)于2023年分别为3880万元及2300万元,占同年研发开支总额的13.7%及8.1%,以及占同年经营开支总额的9.4%及5.6%;(ii)于2024年分别为810万元及3520万元,占同年研发开支总额的4.0%及17.1%,以及占同年经营开支总额的2.0%及8.5%;及(iii)于截至2025年3月31日止三个月分别为60万元及970万元,占同期研发开支总额的1.2%及20.9%,以及占同期经营开支总额的0.7%及11.7%。
招股书显示,公司业务及行业相关的风险(部分):
1、新疫苗产品的开发较复杂,具有不确定性且耗时耗资
2、公司可能无法根据适用的监管要求获得在研疫苗的监管审批。监管机构拒绝或延迟授予任何有关批准均可能导致公司在研疫苗的开发及商业推广推迟,并对公司的营收潜力、业务及经营业绩产生不利影响
3、公司在研疫苗早期研究及试验的结果未必能预测未来试验结果,且完成临床试验并不保证在研疫苗获得监管审批。
4、公司的疫苗可能引发不良副作用或具有其他特性,这可能会延迟或阻碍疫苗获得监管审批,限制获批标签的商业应用,或者在获得上市批准(如有)后导致重大负面后果。
5、公司委聘CRO开展部分临床试验相关活动,但其不受公司控制。
6、公司的全部收入、利润及现金流均来自四价流感病毒亚单位疫苗。其收入降低可能对公司的业务、财务状况、经营业绩及前景造成不利影响。
公司募资用途:
1、将分配至公司的核心产品的开发及国内外注册
2、将用于公司的其他在研疫苗的开发和注册
3、将分配至改进公司的工艺及商业化能力
4、将分配至公司的技术平台的开发
5、将分配至营运资金及其他一般公司用途