今年以来,创新药市场交易火热,据医药魔方,2025H1,中国创新药License out总金额接近660亿美元,赶超2024全年BD交易总额。免疫系统药物是仅次于肿瘤的全球第二大处方药物市场,BD的占比在提升,2023年至2024年,肿瘤管线出海授权交易占比从72%下降至61%,而代谢和自免占比从12%提升至25%。
今年以来,市场表现最亮眼的主要集中在IO上,例如三生制药(01530)、荣昌生物(09995)年内涨幅超3倍,康方生物(09926)涨幅亦接近1.5倍,反观免疫药如康诺亚-B(02162)年内涨幅仅接近90%,二级市场上表现差距甚远。
那么作为全球第二大处方药物市场,免疫药能否接力下一个IO呢?
自免领域迈入双抗时代,下一个大爆款或将诞生
自身免疫病是由机体免疫系统错误攻击自身健康组织所引起的疾病,通常病程漫长、反复发作,因此又被称为“不死的癌症”。这些疾病一般不会直接威胁生命,但常常严重影响患者的生活质量。尽管目前已有一些治疗手段可以减轻症状,但是缺乏根治方法。
尤其是对于系统性红斑狼疮(SLE)、类风湿性关节炎(RA)等常见的自免疾病,导致巨大的用药需求和持续的治疗周期。因此,自免疾病领域因其庞大的市场需求和未被满足的治疗需求,已成为医药行业中备受关注、极具发展潜力的重点领域。据Business Research insights预计,到2027年全球自身免疫性疾病治疗市场规模将达到1193.5亿美元。
曾几何时,免疫市场亦诞生销售过千亿美金的药王。从2003年产品上市开始,艾伯维TNFα抑制剂修美乐(阿达木单抗)作为免疫领域当之无愧的龙头,力压1998年上市的类克(英夫利昔单抗,由强生/默沙东/田边三菱负责销售)和恩利(依那西普,由安进/辉瑞负责销售)这两款TNFα产品,以及诸多生物类似物。修美乐直到2023 年1月专利到期之前,累计20年整个生命周期贡献超过2000亿美元收入,大致获批了16种适应症。TNFα抑制剂整体生物制剂市场,三家主打专利药单年最高曾接近350亿美元销售额,可以称得上是创新药史上最成功的靶点。
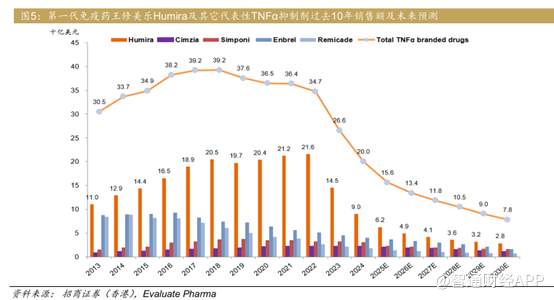
免疫用药市场从TNFα抑制剂开启,吸引更多研发者投入资金,对这类型疾病的机制进行深度的医学探索和市场开拓。
在以上三款超级单品之后,比利时UCB公司希敏佳Cimzia(培塞利珠单抗)上市,用于克罗恩病,强生继续推出一款TNFα抑制剂欣普尼Simponi (戈利木单抗)。
但是不论是UCB公司的Cimzia,还是强生的Simponi,都未能复制曾经三款TNFα抑制剂的辉煌,目前的销售额均在30亿美元以下,峰值也并未超过35亿美元。
修美乐之后,免疫领域新靶点争相涌现(白介素类、JAK/Tyk2抑制剂等),且专利药物数量也远多过TNFα三国时代,单款专利药的适应症数量也很难超过8种,说明在后一阶段的临床及商业化竞争中,市场愈加白热化,临床上精准治疗的理念逐渐加深。
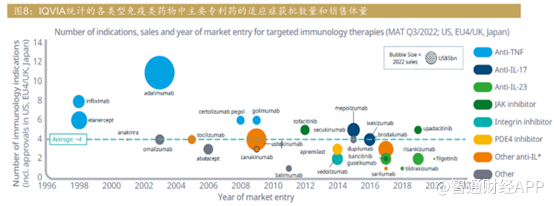
目前单抗药物在一些自身免疫疾病中已经表现出优异的疗效,但仍有部分疾病如COPD、IBD等需要更好的治疗手段,因此双特异性抗体药物治疗自身免疫疾病的研究逐渐兴起。
双抗药物的核心特点在于能够同时靶向两个不同的抗原或表位,更有效地抑制疾病进程,还可以设计出同时抑制过度活化的免疫细胞和促进调节性细胞的功能,更精准地恢复免疫耐受;此外,双抗药物还可以诱导特定的细胞间相互作用,即细胞桥接。这种“桥接”可以将效应细胞直接“招募”到靶细胞附近,实现精确的细胞杀伤或调节,在自免疾病治疗中体现为招募T细胞杀伤异常活化的B细胞、浆细胞等。
双抗药物能够同时靶向两个不同的抗原或表位,如TL1A/THFα、TSLP/IL-13、IL-17A/IL-17F,产生叠加或抑制效应,阻断多个致病通路,更有效地抑制疾病进程。这种双重作用机制使得双抗药物在治疗自身免疫疾病时,能够更全面地干预病理过程,从而提高治疗效果;同时T细胞衔接器(TCE)等双抗可以发挥其细胞桥接功能,连接T细胞与异常B细胞,实现对B细胞的精准清除。罗氏研发的莫妥珠单抗(CD3/CD20双抗)临床数据表示,在难治性SLE患者中,CD3/CD20双抗单次高剂量治疗可清除外周血B细胞达200天以上(高剂量组),显著优于CD20单抗(如利妥昔单抗)数周至数月的效果。
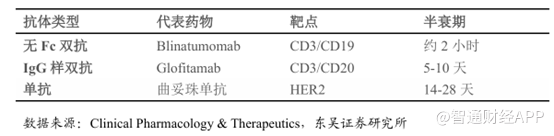
因此,在免疫领域,双抗药市场亦大有可为。
就慢阻肺(COPD)这一适应症而言,传统的LAMA/LABA/ICS三联疗法以缓解症状为主,但无法逆转肺功能下降问题。单抗靶向药(如度普利尤单抗、特泽鲁单抗)精确作用于COPD炎症级联反应中的关键细胞因子、受体或免疫细胞,显著减少嗜酸性粒细胞数量,从而缓解2型炎症,长期改善患者症状。而双抗药物通过抑制炎症启动(TSLP)和下游效应(IL-13),有望比单靶点药物(如IL-4Rα单抗)更彻底地控制2型炎症。
在竞争格局上,康诺亚研发的CM512进度最快已于今年3月25日进入Ⅱ期临床阶段。在COPD和哮喘的动物模型中,CM512显著降低了气道炎症、黏液高分泌和组织纤维化等病理特征。尤其对嗜酸性粒细胞浸润和Th2型炎症反应的抑制效果突出。
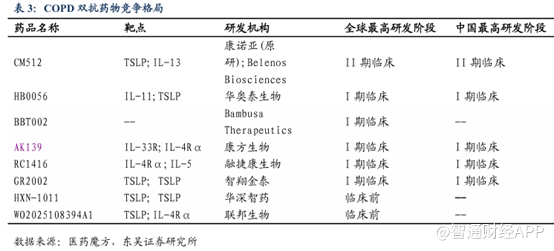
目前双抗自免药物在COPD领域仍处于研发阶段,需要进一步的临床试验证明其可靠性与有效性。
值得一提的是,前几天恒瑞医药的HRS-9821(PDE3/4抑制剂)以及其他11个临床前分子的大中华区以外权益授权给GSK,恒瑞医药获得5亿美元首付款和120亿美元的里程碑付款,合计125亿美元的总交易对价。倘若双抗自免药物在COPD领域获得成功,那么免疫领域有望诞生下一个超级大单品。
康诺亚:核心药物CM310能否进医保是关键
目前国内布局自免领域的药企众多,康诺亚可以说是这一领域的“药王”。在IL-4Rα、CLDN18.2、CD3等多个领域布局了高潜力管线,其中,核心产品司普奇拜单抗(CM310)是国产首家获批的IL-4Rα抗体药物,已进入商业化阶段。
尽管康诺亚的CM310已经商业化,但从其业绩来看,2024年销售收入仅4300万元,扣除分销商折扣及降价补贴后,销售净额为3600万元。
作为康诺亚首个获得监管批准上市的药物,CM310用于治疗多种过敏性疾病,其成人中重度特应性皮炎(AD)适应症于 2024年 9 月 12 日获批上市,成为国内首个、全球范围第二个获批上市的 IL-4Rα 抗体药物,慢性鼻窦炎伴鼻息肉适应症也于2024年12月获批,CM310为国内首款获批此适应症的生物制剂。针对鼻科的慢性鼻窦炎伴鼻息肉(CRSwNP)和季节性过敏性鼻炎(SAR)是国内唯一获批品种,和赛诺菲旗下重磅药物达必妥形成差异化竞争。其中,针对SAR的三期临床数据发表在2025年4月权威期刊《自然医学》杂志,这是全球首个针对SAR疾病的IL-4Rα三期临床研究。
就AD适应症而言,CM310的直接竞争对手为度普利尤单抗。
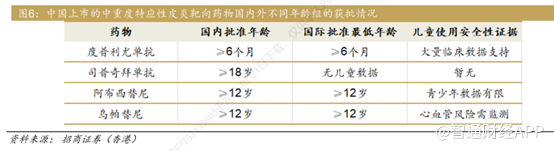
据智通财经APP了解,自从上市以来度普利尤单抗的价格总体呈现下降趋势:2020年7月在国内刚上市时,度普利尤单抗规格为300mg/支,每支价格高达6666元;2021年3月被纳入医保目录后,该药同规格价格降为每支3160元;2023年1月医保续约时,该药同规格价格进一步降至2780元;去年11月28日,度普利尤单抗医保成功续约,价格已降至同规格约1508元。
由于获批较晚,CM310未能赶上去年的医保谈判,进医保前,CM310的医保前300mg商业化的价格为每支单价1659元。相比之下,2025年患者选择度普利尤单抗在经医保报销后,自费部分每支仅450元左右,若按每月两支的常规用量计算,月自费花销仅900元左右,用药成本远低于司普奇拜单抗。因此,今年年底能否进入医保谈判,进而放量对于康诺亚而言至关重要。
此外,国内还有康乃德/先声乐德奇拜单抗(CBP-201),智翔金泰,麦济、恒瑞医药(SHR-1819),三生国健(SSGJ-611)和康方(AK120)等多家公司针对IL-4Rα靶点在AD等领域进行开发,但无论是开发进度,还是临床效果,目前来看对比CM310均处于劣势。乐德奇拜单抗(CBP-201)刚刚提交上市申请,其它IL-4Rα类单抗仍处于临床三期。
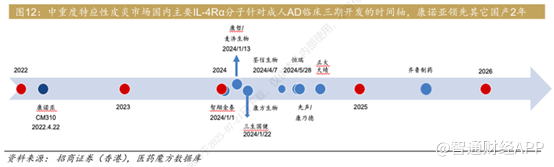
值得一提的是,无论是鼻窦炎伴鼻息肉还是季节性过敏性鼻炎,目前在国内CM310是独家获批的生物制剂,这是CM310对比赛诺菲的达必妥有较大领先的适应症,这也突出了康诺亚在临床开发上的侧重点。
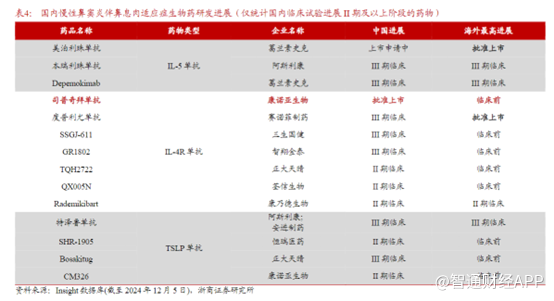
如此来看,在AD这一适应症,康诺亚的CM310在上市后2年内,国内市场上主要与度普利尤单形成正面的竞争关系,今年年底的医保谈判对其至关重要;而在鼻窦炎伴鼻息肉还是季节性过敏性鼻炎这俩适应症上,CM310短期内不会面临市场竞争的压力。招商证券(香港)认为凭借目前批准的三个适应症,CM310到2030年在中国有望接近50亿销售,其管理层亦对CM310前景十分乐观,维持此前披露的2025年CM310销售收入5亿元指引及之前所述的长期销售峰值目标50亿元。
当然,除了CM310这一核心产品外,在肿瘤领域,康诺亚亦有看点,其CMG901全球领先。CMG901是CLDN18.2靶向ADC药物,目前全球范围内暂无上市。国内看:康诺亚 CMG901、信达生物IBI343、恒瑞 SHR-A1904、石药SYSA1801以及礼新医药的LM-302临床进度位于前列,最快适应症已进入III期临床阶段。科伦博泰生物、荣昌生物等紧随其后,进入I/II期临床阶段,布局适应症主要围绕胃癌/胃食管交界处癌以及胰腺癌。海外看:康诺亚临床进度最快,德琪医药处于II期临床阶段,恒瑞医药、科伦博泰、Sotio及荣昌生物进入 I/II 期临床阶段,海外竞争格局较好。

眼下,国内创新药BD火热,而康诺亚对外授权收入亦不低,在2024年4.28亿元的营收中,对外授权合作的收入高达3.92亿元,占比91.6%。
不过与多数创新药License out不同,康诺亚采用的是NewCo模式,并且上述的交易额是在半年时间内完成的。
相比于传统的License out模式,NewCo模式对国内的Biotech公司似乎更加友好。从模式上看,一方面NewCo模式可以在MNC对引进资产的严格把控之下,另辟蹊径为创新药企业提供现金流支持,促进公司自身潜力管线的研发和临床研究;另一方面该模式还能够在一定程度上分散本土药企风险。
另一方面,从过往的一级市场实践来看,一个投后估值1亿-1.5亿美元的NewCo,对应融资金额在8000万美元至1亿美元,经过2-3年左右的运营,退出期望值可以达到10-15亿美元。有临床II期数据的管线,并购价格基本都在10亿美元左右。
因此,在上述估值路径下,康诺亚连续4次达成NewCo协议,足以证明其在该模式下的出海潜力,由此为公司带来持续的估值溢价。
综上来看,自身免疫疾病领域凭借其庞大的市场需求和尚未被充分满足的治疗需求,已成为医药行业中备受瞩目、发展潜力巨大的重点领域。当前,该领域已迈入双抗时代,首款自免双抗药物有望在自免领域创造下一个爆发点。作为国内自免领域的领先企业,康诺亚在自免双抗的研发布局中占据领先地位。其核心品种CM310如能于年底顺利通过医保谈判,在AD适应症上目前竞争者仅度普利尤,市场竞争格局良好,有望通过医保获得放量,为康诺亚带来不错的业绩收益;而其在慢性鼻窦炎伴鼻息肉和季节性过敏性鼻炎等适应症上,则面临相对更良好的市场竞争格局。此外,其在抗肿瘤ADC药物CMG901上的全球开发进展也处于领先位置。
在国内创新药BD热潮的背景下,康诺亚通过NewCo的模式推进国际化战略,这一布局也有望为其市场估值打开进一步上升的空间。